Как вылечить эндометрит при саркоидозе
Хронический эндометрит: от совершенствования диагностического подхода к оптимизации лечения
Хронический эндометрит (ХЭ)— клинико-морфологический синдром, при котором в результате персистирующего повреждения эндометрия инфекционным агентом возникают множественные вторичные морфофункциональные изменения, нарушающие циклическую трансформ
Хронический эндометрит (ХЭ)— клинико-морфологический синдром, при котором в результате персистирующего повреждения эндометрия инфекционным агентом возникают множественные вторичные морфофункциональные изменения, нарушающие циклическую трансформацию и рецепторный статус слизистой оболочки тела матки.
С позиций общей патологии течение инфекции с тенденцией к хронизации можно было бы отнести к «синтаксическим» вариантам, при которых биосистема «…предпочитает существовать с патогеном, активное отторжение которого сопряжено с большими трудностями, энергетически не выгодно или вообще нереально в силу специфики пускового фактора». Наиболее устоявшейся на сегодняшний день является точка зрения о возникновении ХЭ в результате дисбаланса между гормональной и иммунной системами организма, с одной стороны, и патогенами— представителями микробиоценоза, с другой.
В современных условиях ХЭ характеризуется рядом особенностей: изменением этиологической структуры с увеличением значимости вирусной и условно-патогенной флоры, ростом резистентности флоры к фармакотерапии, трансформацией клинической симптоматики в сторону стертых форм и атипичного течения, длительными сроками терапии и ее высокой стоимостью. В 95% случаев эндометрит является экзогенным (первичным), вызванным штаммами микроорганизмов, передающихся половым путем, а также возникающим после внутриматочных лечебных и диагностических манипуляций. Лишь в 5% случаев эндометрит является вторичным и развивается при попадании инфекции из экстрагенитальных очагов гематогенным, лимфогенным или нисходящим путем. «Интегральными» возможно назвать клинические классификации ХЭ (C. Buckley, H. Fox (2002) и T.C.Michels (1995)). Согласно им выделяют специфический (обусловленный бактериальной флорой, вирусами, грибами, хламидиями, микоплазмами) и неспецифический варианты ХЭ, при котором специфическая флора из эндометрия не выделяется.
Поддержание стерильности эндометрия за счет циклического отторжения функционального слоя во время менструации на протяжении нескольких десятилетий заставляло исследователей сомневаться в существовании хронической формы эндометрита. В дальнейшем было доказано вовлечение в хронический воспалительный процесс не только функционального, но и не отторгающегося базального слоя эндометрия.
Изучение микробного пейзажа эндометрия имеет сравнительно недолгую историю. Факт персистирования микоплазмы в эндометрии упоминается впервые в работе Koren Z. (1978). В эндометрии обнаружена персистенция более 20 видов микроорганизмов условно-патогенной группы. Всего выделено 129 штаммов, в том числе облигатные анаэробы— 64% (бактероиды, эубактерии, пептострептококки, клостридии), микроаэрофилы— 31,8% (генитальные микоплазмы и дифтероиды), факультативные анаэробы— 12%. Только у 14% женщин выделены монокультуры, у остальных обнаружены ассоциации 2–6 видов микроорганизмов. Вполне возможно, что антиген персистирующей инфекции «запускает» иммунный ответ с реакцией гиперчувствительности замедленного типа. Из числа обследованных нами пациенток с предшествующими неудачами экстракорпорального оплодотворения (ЭКО) и морфологически подтвержденным ХЭ у 76% при микробиологическом исследовании содержимого полости матки был выявлен возбудитель инфекционного процесса (Enterococcus fecalis— 20%, Staphylococcus epidermidis— 28%, Staphylococcus spp. — 16%, Ureaplasma urealyticum— 24%, вирус простого герпеса (ВПГ)— 12%, цитомегаловирус (ЦМВ)— 8%, в большинстве случаев наблюдались ассоциации микроорганизмов), у 24% пациенток проведенное исследование не позволило выявить возбудителя.
Защитные механизмы при внутриматочной инфекции делят на специфические и неспецифические. Среди неспецифических антимикробных механизмов, действующих на клеточном уровне, следует отметить фагоцитоз с помощью макрофагов и полиморфноядерных лейкоцитов. Неспецифические гуморальные факторы включают белок плазмы трансферрин, связывающий железо, необходимое для роста многих бактерий; опсонины, усиливающие фагоцитарную активность клеток; лизоцим цервикальной слизи, бетализин, выделяющийся тромбоцитами в очаге воспаления. К специфическим факторам защиты относят: Т-лимфоциты, иммуноглобулины. Однако, несмотря на достаточно четкие представления о секреторной иммунной системе слизистых оболочек пищеварительного тракта и дыхательных путей, сведения об иммунной системе эндометрия и ее значении для женских половых путей остаются немногочисленными.
Широко освещен в литературе вопрос факторов риска развития ХЭ. По нашим данным, наиболее значимыми (р
Е. Б. Рудакова, доктор медицинских наук, профессор А. А. Лузин, О. Н. Богданова, С. И. Мозговой, кандидат медицинских наук, доцент, О. А. Лобода, М. А. Пилипенко, О. М. Бурова ОмГМА, ОмОКБ, ОмЦРМ, Омск.
Эндометрит: симптомы и лечение у женщин
Что такое эндометрит матки?
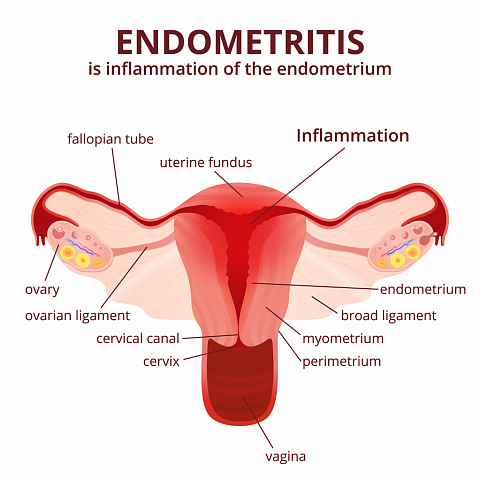
Эндометритом называется воспаление слизистой оболочки матки, которое начинается из-за паразитирования микроорганизмов: они повреждают слизистую, активируют иммунную систему и мигрируют в область воспаления. Есть несколько видов таких «вредителей»:
Симптомы и лечение эндометрита связаны со сложностью заболевания. При тяжелом течении эндометрита (помимо стандартного воспаления) развивается гнойный процесс. Гной образуется из погибших «бойцов» в борьбе за здоровье организма — микроорганизмов и лейкоцитов — и значительно утяжеляет течение заболевания. Иногда у больных проявляется пиометра — состояние, при котором полость матки заполняется гноем.
Возбудители проникают в матку двумя путями: восходящим и нисходящим. В первом случае бактерии попадают в полость из влагалища через шейку матки. Нисходящий путь бывает гематогенным или лимфогенным: иными словами, если в организме уже запущен какой-то воспалительный процесс, возбудитель попадает в матку через кровь или лимфу.
На развитие и течение воспаления влияет ряд провоцирующих факторов:
Другие, не менее опасные факторы — появление в полости матки остатков плаценты после кесарева сечения или родов, а также наличие там децидуальной (отпадающей) ткани, сгустков крови, плодного яйца. Поэтому аборт (особенно в нестерильных условиях) и выскабливание могут привести к воспалению.
Симптомы эндометрита матки
Лейкоциты — клетки иммунной системы — вырабатывают медиаторы воспаления простагландины. Этот процесс проявляется в ряде симптомов:
При эндометрите проявляется острое либо хроническое воспаления: первое характеризуется яркой симптоматикой, второе нередко протекает бессимптомно. Острый воспалительный процесс чаще связан с воздействием сразу нескольких микроорганизмов. Реже слизистая оболочка поражается изолированно: обычно воспаляется мышечная оболочка матки наравне с развитием миоэндометрита.
При остром эндометрите симптомы проявляются на 3-4 день: повышается температура, наблюдается слабость, головная боль и боль внизу живота, гнойные и (или) кровянистые выделения. Острая стадия длится от 8 до 10 дней и полностью проходит при правильном и своевременном лечении. Если же этого не произошло, острая форма может перетечь в хроническую.
Хронический эндометрит легко не заметить: часто женщины узнают о заболевании только на приеме у гинеколога или при планировании беременности. Наиболее яркий симптом заболевания — нарушение менструального цикла. Температура у пациенток обычно нормальная, иногда бывают ноющие боли в пояснице и внизу живота. Поэтому окончательный диагноз ставится только на основе гистологического исследования эндометрия.
При обсуждении репродуктологии важнее говорить о хроническом эндометрите (ХЭ). Острая патология замечается почти сразу и потому оперативно устраняется. А вот хроническая фаза требует долгого лечения в течение нескольких месяцев, ведь при такой форме заболевания эндометрий сильно видоизменяется, не может трансформироваться и обновляться.
Чаще всего болезнь проявляется у женщин от 26 до 35 лет. Национальный центр контроля заболеваемости сообщает, что каждый год в США регистрируют около 1 млн воспалительных заболеваний органов малого таза. В России такие диагнозы ставятся от 28 до 34 % пациенток гинекологии. При хроническом эндометрите часто развивается бесплодие или привычное невынашивание беременности: до 65 % и до 70 % случаев соответственно. Плодное яйцо не может прикрепиться к измененному эндометрию, из-за чего беременность не наступает или протекает неудачно.
Клинические проявления хронического эндометрита таковы:
Однако единого мнения насчет клинической картины хронического эндометрита не существует. Даже при явных симптомах невозможно понять, какова глубина функциональных и структурных изменений эндометрия.
Лечение эндометрита у женщин разного возраста
Симптомы и лечение эндометрита у женщин мало связаны с возрастом. После 40 лет острый эндометрит обычно проявляется более ярко: на это влияют изменения гормонального фона из-за предстоящего климакса. Переход острой формы в хроническую в этом возрасте происходит намного быстрее, однако формат лечения в 25 и 45 лет не различается.
Борьба с заболеванием — сложная, но важная задача, особенно у женщин, переживших выкидыш или неудачное ЭКО. Чтобы поставить точный диагноз и подобрать индивидуальное лечение, врачи МЦРМ собирают детальный анамнез. Необходимо выяснить информацию о менструальной функции, течении и исходе беременностей, абортах и выкидышах. Это позволит верно диагностировать патологию и подготовить эндометрий к беременности с помощью специально подобранных препаратов.
В комплексное лечение входят антибиотики широкого спектра с высокой способностью проникновения в клетку, а также (в зависимости от вида возбудителя) противогрибковые (антимикотики) и противовирусные препараты, местные комбинированные лекарства, системная энзимотерапия (применение ферментов) и физиотерапия в момент реабилитации. Для профилактики кандидоза на фоне антибиотиков назначаются противогрибковые препараты.
Следующий этап — гормональная терапия: комбинированные оральные контрацептивы. Во вторую фазу цикла при планировании беременности врач назначает прогестерон. Лечение начинается с первого дня менструации.
Перед назначением препаратов в нашей клинике проходит комплексная диагностика:
После диагностики мы подбираем индивидуальное лечение. На первом этапе необходимо уничтожить инфекционного агента, на втором — восстановить функционал эндометрия: благодаря лечению устраняются повреждения, завершается регенерация, восстанавливается локальная гемодинамика (движение крови в сосудах) и активность рецепторов эндометрия.
В стенах клиники мы много лет разрабатывали схемы, которые помогают наиболее эффективно бороться с заболеванием. Прежде всего на весь период лечения (два-три менструальных цикла) прописываются следующие препараты:
Препараты в первый месяц лечения:
1. При обнаружении патогена по результатам фемофлор-скриннинга с первого дня менструального цикла назначается антибактериальная либо противовирусная терапия — в зависимости от вида возбудителя. Если в результате фемофлор-скрининга патоген не найден, антибиотики пить не нужно!
2. Также важна поддержка нормальной флоры желудочно-кишечного тракта и влагалища, поэтому:
Препараты во второй месяц лечения:
1. Активная иммунотерапия: 10 дней после менструации принимается Генферон — 250 тыс. ед. два раза в сутки интравагинально.
2. Препараты, которые активируют обмен веществ в тканях, улучшают трофику (питание клеток) и стимулируют процесс регенерации: Актовегин — одно драже 3 раза в сутки перед приемом пищи на протяжении 30 дней.
3. Физиотерапевтические методы благоприятно влияют на пораженные ткани, помогают снять воспалительные процессы, улучшить состояние сосудов и эндометрия.
В третий месяц лечения важно закрепить результат: лучше всего отправиться на санаторно-курортное лечение. Можно поехать в «Балтийский Берег» в Зеленогорске (50 км от центра Санкт-Петербурга): там работают врачи-партнеры, сопровождающие наших пациентов на месте. Специалисты будут знать всё о вашем диагнозе и дадут своевременный совет. Стоимость индивидуальной программы составляет от 2060 рублей в сутки.
Хронический эндометрит и беременность
Как уже было сказано ранее, при хроническом эндометрите часто наблюдается бесплодие или привычное невынашивание беременности. Необходимо, чтобы слой эндометрия постоянно регенерировался: только тогда зародыш будет успешно имплантирован в матку. При хроническом эндометрите регенерация невозможна из-за воспалительного процесса, поэтому плодное яйцо не может закрепиться на эндометрии.
Даже если это происходит, беременность редко оказывается успешной: риск выкидыша сохранится на протяжении вынашивания. Такую беременность сопровождают нарушения и осложнения: в частности, возбудители заболевания могут поразить ткани плода, что приведет к его гибели.
Нарушение развития эмбриона — еще одно возможное последствие беременности при эндометрите. Поврежденному эндометрию не хватает поступления крови из-за застоя: ткань не получает кислород, витамины, питательные вещества и не передает их эмбриону. Из-за этого ребенок может родиться с патологиями. Кроме того в несколько раз повышается вероятность рождения раньше срока, может нарушиться формирование плаценты, так что при планировании беременности следует немедленно начать лечение этого заболевания.
В общей сложности выкидыши и бесплодие из-за хронического эндометрита связаны сразу с несколькими причинами:
Поэтому перед планированием беременности необходимо пройти полный курс лечения от эндометрита: в таком случае вероятность забеременеть может возрасти до 100 %. В случае с ЭКО основная проблема связана именно с закреплением половых клеток в матке, поэтому для эффективности стоит сделать несколько попыток подсадить оплодотворенную яйцеклетку. Помимо приема препаратов необходимо поберечь себя: постараться исключить стрессы, ограничить физическую нагрузку и не поднимать тяжести.
Как вылечить эндометрит при саркоидозе
Кафедра акушерства, гинекологии и перинатологии медицинской академии им. С.И. Георгиевского ФГАОУ ВО «Крымский федеральный университет им. В.И. Вернадского» Министерства образования и науки Российской Федерации, Симферополь, Россия
Кафедра акушерства, гинекологии и перинатологии медицинской академии им. С.И. Георгиевского ФГАОУ ВО «Крымский федеральный университет им. В.И. Вернадского» Министерства образования и науки Российской Федерации, Симферополь, Россия
Кафедра акушерства, гинекологии и перинатологии медицинской академии им. С.И. Георгиевского ФГАОУ ВО «Крымский федеральный университет им. В.И. Вернадского» Министерства образования и науки Российской Федерации, Симферополь, Россия
Кафедра акушерства, гинекологии и перинатологии медицинской академии им. С.И. Георгиевского ФГАОУ ВО «Крымский федеральный университет им. В.И. Вернадского» Министерства образования и науки Российской Федерации, Симферополь, Россия
Кафедра акушерства, гинекологии и перинатологии медицинской академии им. С.И. Георгиевского ФГАОУ ВО «Крымский федеральный университет им. В.И. Вернадского» Министерства образования и науки Российской Федерации, Симферополь, Россия
Кафедра акушерства, гинекологии и перинатологии медицинской академии им. С.И. Георгиевского ФГАОУ ВО «Крымский федеральный университет им. В.И. Вернадского» Министерства образования и науки Российской Федерации, Симферополь, Россия
Хронический эндометрит: современное состояние проблемы, основные аспекты патогенеза, влияние на репродуктивную функцию
Журнал: Российский вестник акушера-гинеколога. 2016;16(5): 37-41
Яковчук Е. К., Сулима А. Н., Рыбалка А. Н., Дижа М. А., Аникин С. С., Симачева С. А. Хронический эндометрит: современное состояние проблемы, основные аспекты патогенеза, влияние на репродуктивную функцию. Российский вестник акушера-гинеколога. 2016;16(5):37-41.
Yakovchuk E K, Sulima A N, Rybalka A N, Dizha M A, Anikin S S, Simacheva S A. Chronic endometritis: State-of-the-art, main aspects of pathogenesis, impact on reproductive function. Russian Bulletin of Obstetrician-Gynecologist. 2016;16(5):37-41.
https://doi.org/10.17116/rosakush201616537-41
Кафедра акушерства, гинекологии и перинатологии медицинской академии им. С.И. Георгиевского ФГАОУ ВО «Крымский федеральный университет им. В.И. Вернадского» Министерства образования и науки Российской Федерации, Симферополь, Россия
Представлен анализ опубликованных работ последних лет, касающийся вопросов этиологии и патогенеза хронического эндометрита. Хронический эндометрит — клинико-морфологический синдром, при котором в результате персистирующего повреждения эндометрия инфекционным фактором возникают множественные вторичные морфофункциональные изменения, нарушающие циклическую биотрансформацию и рецептивность слизистой оболочки тела матки. Среди женщин с верифицированным хроническим эндометритом у 60% диагностируется бесплодие. Особенностями хронического эндометрита в настоящее время являются увеличение значимости условно-патогенной микрофлоры, рост устойчивости условно-патогенных микроорганизмов к фармакотерапии, увеличение числа стертых форм и атипичного течения. При реализации хронического воспалительного процесса в эндометрии на клеточном уровне происходят следующие нарушения: расстройства метаболизма, нарушение цепи иммунокомпетентной системы и развитие аутоиммунных процессов, нарушение эспрессии рецепторов стероидных гормонов, формирование провоспалительного Th-1-типа имунного ответа вместо необходимого для успешного развития беременности Th-2-типа такого ответа, ухудшение микроциркуляции, нарастание гипоксии, дисбаланса про- и антиоксидантной систем. Авторы информируют об отсутствии конфликта интересов.
Кафедра акушерства, гинекологии и перинатологии медицинской академии им. С.И. Георгиевского ФГАОУ ВО «Крымский федеральный университет им. В.И. Вернадского» Министерства образования и науки Российской Федерации, Симферополь, Россия
Кафедра акушерства, гинекологии и перинатологии медицинской академии им. С.И. Георгиевского ФГАОУ ВО «Крымский федеральный университет им. В.И. Вернадского» Министерства образования и науки Российской Федерации, Симферополь, Россия
Кафедра акушерства, гинекологии и перинатологии медицинской академии им. С.И. Георгиевского ФГАОУ ВО «Крымский федеральный университет им. В.И. Вернадского» Министерства образования и науки Российской Федерации, Симферополь, Россия
Кафедра акушерства, гинекологии и перинатологии медицинской академии им. С.И. Георгиевского ФГАОУ ВО «Крымский федеральный университет им. В.И. Вернадского» Министерства образования и науки Российской Федерации, Симферополь, Россия
Кафедра акушерства, гинекологии и перинатологии медицинской академии им. С.И. Георгиевского ФГАОУ ВО «Крымский федеральный университет им. В.И. Вернадского» Министерства образования и науки Российской Федерации, Симферополь, Россия
Кафедра акушерства, гинекологии и перинатологии медицинской академии им. С.И. Георгиевского ФГАОУ ВО «Крымский федеральный университет им. В.И. Вернадского» Министерства образования и науки Российской Федерации, Симферополь, Россия
Среди супружеских пар детородного возраста частота бесплодия в разных регионах России колеблется от 8 до 19%. Восстановление репродуктивной функции в условиях сложной демографической ситуации в стране — задача, выходящая за рамки только медицинской науки. В связи с этим к вспомогательным репродуктивным технологиям (ВРТ) проявляют повышенный интерес не только в России, но и за рубежом. Во многих странах эффективность результатов экстракорпорального оплодотворения (ЭКО) и переноса эмбрионов (ПЭ) определяется двумя факторами — функциональной полноценностью эмбриона на стадии бластоцисты и отсутствием внутриматочной патологии. Одной из главных причин неполноценной или неудачной имплантации являются нарушенная функция и поврежденная структура эндометрия, часто обусловленная хроническим воспалительным процессом в эндометрии.
Хронический эндометрит (ХЭ) — клинико-морфологический синдром, при котором в результате персистирующего повреждения эндометрия инфекционным фактором возникают множественные вторичные морфофункциональные изменения, нарушающие циклическую биотрансформацию и рецептивность слизистой оболочки тела матки [1].
Вопрос о необходимости выделения ХЭ как воспалительного процесса во внутренних слоях матки в отдельную нозологическую единицу долгое время обсуждался в научной среде в связи со способностью функционального слоя эндометрия к отторжению во время менструации. Существовали два разнонаправленных мнения о роли инфекционного агента в генезе Х.Э. Некоторые исследователи [2] придерживались точки зрения, что полость матки стерильна, и в случаях проникновения в эндометрий условно-патогенной микрофлоры (УПМ) примерно в 60% возникает патологический процесс. Другие исследователи [3] утверждали, что слизистая оболочка матки не может быть стерильной из-за перманентной микробной колонизации из нижних отделов полового тракта.
Изучение микробного пейзажа эндометрия имеет сравнительно недолгую историю. О персистировании микоплазмы в эндометрии упоминается впервые в работе Z. Koren (1978) [цит. по 4]. В эндометрии обнаружена персистенция более 20 видов микроорганизмов условно-патогенной группы. Всего выделено 129 штаммов, в том числе облигатные анаэробы — 64% (бактероиды, эубактерии, пептострептококки, клостридии), микроаэрофилы — 31,8% (генитальные микоплазмы и дифтероиды), факультативные анаэробы — 12%. Только у 14% женщин выделены монокультуры, у остальных обнаружены ассоциации 2—6 видов микроорганизмов.
В настоящее время ХЭ выделен как самостоятельная нозологическая единица в Международной классификации болезней и причин смерти 10-го пересмотра: класс XIV. N071.1. [5].
Распространенность ХЭ варьирует от 10 до 85%, что связано с трудностями диагностики, клинической и морфологической верификации заболевания [6]. По различным данным, среди больных с бесплодием число случаев ХЭ составляет в среднем 10% (от 7,8 до 15,4%). В 80—90% ХЭ выявляется у женщин детородного возраста (средний возраст заболевших — 36 лет) и обусловливает у них нарушения менструальной и репродуктивной функций, приводя, в конечном итоге, к развитию бесплодия, неудачам в программах ЭКО и ПЭ, невынашиванию беременности и осложненному течению гестационного процесса и родов [7].
Среди женщин с верифицированным ХЭ у 60% диагностируется бесплодие (в 22,1% — первичное, в 36,5% — вторичное), неудачные попытки ЭКО и переноса эмбрионов в анамнезе отмечены у 40% женщин. У пациенток с несколькими неудачными попытками ЭКО в анамнезе распространенность ХЭ достигает 80%, причем среднее количество неудач в программах ВРТ приблизительно равняется 3 на одну женщину. По другим данным [8], ХЭ является единственной диагностированной причиной невынашивания беременности в 47,4—52,1%.
В 95% ХЭ является первичным, развиваясь непосредственно в эндометрии за счет внедрения экзогенных штаммов микроорганизмов, передаваемых половым путем, или размножения УПМ в эндометрии после внутриматочных лечебных и диагностических манипуляций. Лишь в 5% эндометрит носит вторичный характер, развиваясь при попадании инфекции в эндометрий из экстрагенитальных очагов гематогенным, лимфогенным или нисходящим путями [9, 10].
В настоящее время широкое распространение получила этиологическая классификация ХЭ [11]. Принято выделять неспецифический и специфический ХЭ. В первом случае специфическая микрофлора в клетках слизистой оболочки тела матки не выявляется. Специфический Х.Э. может быть хламидийной, вирусной (вирус простого герпеса — ВПГ, цитомегаловирус — ЦМВ, энтеровирусы), бактериальной (возбудители туберкулеза, гонореи, менингита, сифилиса), микоплазменной, грибковой, протозойной (токсоплазма, шистосома) и паразитарной этиологии, а также может развиваться на фоне саркоидоза.
Спектр генитальной инфекции, выявленной при ПЦР-диагностике отделяемого из цервикального канала и полости матки у пациенток с ХЭ, включает: уреаплазмоз — в 37,8%, генитальный герпес — в 33,6%, ЦМВ — в 18,9% случаев, хламидиоз — в 14,9%, микоплазмоз — в 11,6% [12].
Факторами риска возникновения ХЭ являются инвазивные манипуляции в полости матки (введение внутриматочных контрацептивов, биопсия эндометрия, выскабливание стенок полости матки, гистероскопия, гистеросальпингография, внутриматочная инсеминация, ЭКО), послеродовые инфекционно-воспалительные осложнения, заболевания мочеполового тракта, хронический сальпингоофорит в анамнезе, инфекции влагалища и цервикального канала, бактериальный вагиноз, деформации полости матки с нарушением циклического отторжения эндометрия, лучевая терапия в области органов малого таза, а также перенесенные операции на органах малого таза [13—15].
Большую и может быть основную роль в генезе развития ХЭ играют социальные факторы: раннее начало половой жизни, частая смена половых партнеров, половые отношения во время менструации, курение, употребление алкоголя [16].
Клиническая картина ХЭ отражает глубину и давность функциональных и структурных изменений в ткани эндометрия. Неполноценная циклическая трансформация эндометрия на фоне воспалительного процесса, нарушение процессов десквамации и регенерации функционального слоя эндометрия приводят к появлению основного симптома заболевания — перименструальных, межменструальных маточных кровотечений. Пациентки могут предъявлять жалобы на тянущие боли внизу живота, дисменорею и диспареунию. В целом у 35—40% пациенток клинические симптомы заболевания отсутствуют и единственным клиническим проявлением ХЭ служит бесплодие или невынашивание беременности [17—19].
В современных условиях ХЭ имеет ряд особенностей: смену этиологических факторов с увеличением роли вирусной инфекции и УПМ, рост устойчивости УПМ к фармакотерапии, изменение клинической симптоматики в сторону увеличения числа стертых форм и случаев атипичного течения, более длительные сроки терапии и ее высокую стоимость [20].
Чаще всего этиологическим фактором ХЭ являются хламидии, микоплазмы и уреаплазмы, вирусы, аэробные и анаэробные бактерии. Инфицирование полости матки происходит за счет проникновения микроорганизмов из нижних отделов генитального тракта с помощью сперматозоидов, трихомонад, пассивного транспорта в результате отрицательного внутрибрюшного давления. Из полости матки больных ХЭ в 28,9% выделены различные виды аэробных микроорганизмов, в основном УПМ. В слизистой оболочке матки выявлены грамположительные палочки, грамположительные и грамотрицательные кокки у 71,1% больных ХЭ при отрицательных результатах бактериологического исследования содержимого полости матки. Отсутствие роста культуры при посеве содержимого полости матки не исключает наличие микроорганизмов в эндометрии, которые поддерживают хроническое течение воспаления. При эндометритах установлена персистенция в эндометрии некоторых микроорганизмов (хламидии, микоплазмы, вирусы и др.). У женщин с бактериальным вагинозом выявлена плазмоклеточная инфильтрация в эндометрии, а также аэробы, анаэробы, хламидии, микоплазмы, уреаплазмы. Рассматривают также наличие «ключевых» клеток в мазках как фактора повышенного риска развития постабортного и послеродового эндометрита [21].
Выявление вирусов регистрируется в 50,7%, чаще всего диагностируют наличие вируса простого герпеса I—II типа, инфекцию, вызванную вирусом папилломы человека 16-го, 18-го типа. На долю микробно-вирусных ассоциаций приходится 52,7%. Наиболее тяжелые морфологические изменения эндометрия наблюдаются при сочетании бактериальной и вирусной инфекции и аутоиммунном поражении эндометрия [8].
Таким образом, развитие ХЭ ассоциировано в основном с УПМ (оппортунистической микрофлорой), активность которой существенно зависит от функций иммунной системы. В то же время многие из этих микроорганизмов обладают выраженным иммуносупрессивным свойством, обеспечивающим латентную персистенцию возбудителя в организме хозяина.
Проведено исследование причин нарушений репродуктивной функции у женщин с нарушениями менструального цикла. Обследованы 2190 женщин, ХЭ диагностирован в 20%. УПМ в слизистой оболочке матки выделена в 54%. При прицельном обследовании женщин с бессимптомным течением ХЭ выделена УПМ у 69% [22].
В группе женщин с ХЭ эндометрий был стерилен лишь в 10%, в 55% была выделена УПМ. Это свидетельствует о том, что ХЭ доминирует у женщин с нарушениями микроэкологии влагалища, перенесших инфекции, передаваемые половым путем (ИППП), и многократные внутриматочные манипуляции в анамнезе. Среди причин возникновения ХЭ преобладала УПМ, этиологически связанная с бактериальным вагинозом (G. vaginalis) и неспецифическим вагинитом [23].
У пациенток с предшествующими неудачами ЭКО и морфологически подтвержденным ХЭ в 76% при микробиологическом исследовании содержимого полости матки был выявлен возбудитель инфекционного процесса (Staphylococcus epidermidis — 28%, Ureaplasma urealyticum — 24%, Enterococcus faecalis — 20%, Staphylococcus spp.— 16%, вирус простого герпеса (ВПГ) — 12%, цитомегаловирус — 8%, в большинстве случаев наблюдаются ассоциации микроорганизмов), у 24% пациенток возбудитель не был выявлен [24].
Существует мнение, что УПМ может длительно персистировать в эндометрии, существуя в форме бактерий с замедленным метаболизмом, низкой скоростью размножения. С этим фактом связана неоднозначность диагностики при выявлении низкого титра выделяемых из эндометрия УПМ. Ученые пришли к выводу, что способность УПМ вызывать ХЭ — полидетерминированное свойство, связанное с действием различных факторов вирулентности и патогенности микроорганизма. Однако в развитии инфекционного процесса ведущая роль принадлежит реактивности организма-хозяина и состоянию локального иммунитета. Персистенция микроорганизмов в эндометрии, относящихся к УПМ, приводит к развитию аутоиммунной реакции за счет антигенов, общих с тканевыми антигенами организма. Возможно образование инфламмасом — белково-макрофагальных комплексов, являющихся компонентом как острого, так и хронического аутоиммунного воспаления [25]. Кроме того, длительная стимуляция иммунокомпетентных клеток эндометрия приводит к декомпенсации регуляторных механизмов локального гомеостаза, что поддерживает инфекционный процесс.
Нет единой концепции патогенеза ХЭ, раскрывающей механизмы формирования и взаимосвязи различных аспектов патогенетической цепи и детально объясняющей патологические основы хронического воспалительного процесса в эндометрии.
В патогенезе неспецифического ХЭ определяющую роль играет постинфекционный аутоиммунный синдром. Он проявляется резким повышением в сыворотке крови уровня аутоантител к белкам эндометрия и провоспалительных цитокинов, продуцентами которых являются Th-1 (фактор некроза опухоли-α и интерферон-γ), увеличением инфильтрации эндометрия CD16+ и CD56+, NK-клетками, В-клетками и активированными лимфоцитами HLA-DR+, а также нарушением экспрессии рецепторов половых стероидов в эндометрии. Все эти изменения в эндометрии ХЭ препятствуют нормальной имплантации и плацентации, способствуют ранним репродуктивным потерям [26].
Бактериально-вирусная колонизация эндометрия является, как правило, следствием неспособности иммунной системы и неспецифических защитных сил организма полностью элиминировать инфекционный агент наряду с ограничением его распространения за счет активации Т-лимфоцитов и макрофагов. В результате возникает персистенция микроорганизмов, характеризующаяся привлечением в очаг хронического воспаления мононуклеарных фагоцитов, естественных киллеров, синтезирующих различные цитокины. В результате иммунопатологичеcких процессов нарушается экспрессия стероидных рецепторов эндометрия.
У женщин с нарушениями репродуктивной функции на фоне ХЭ прослежена тенденция к снижению экспрессии прогестероновых рецепторов как на этапе их формирования в пролиферативной фазе, так и в период «окна» имплантации, что и следует рассматривать как один из патогенетических этапов развития привычного невынашивания беременности. Воспалительный процесс в эндометрии, проявляющийся четкими морфологическими изменениями на 6—9-й день менструального цикла, изменяет формирование рецепторов эстрогенов и прогестерона, и эта тенденция нарастает в секреторной фазе менструального цикла. Снижение прогестероновой рецепции, вероятно, и приводит к нарушению нормальной дифференцировки эндометрия и вызывает активную пролиферацию за счет сохраненного уровня экспрессии эстрогеновых рецепторов во всех компонентах эндометрия. Это подтверждает, что ведущим механизмом формирования и развития пролиферативных процессов в матке является нарушение экспрессии рецепторов стероидных гормонов [27, 28].
При изучении ХЭ с аутоиммунным компонентом обратили внимание на отставание секреторной трансформации эндометрия при полноценной гормональной активности желтого тела с нормальным содержанием прогестерона в крови. Не исключено, что антиэндометриальные антитела могут оказывать самостоятельное влияние на гормонрецепторные взаимодействия в ткани эндометрия, нарушая морфофункциональное состояние эндометрия [16].
Известны более 30 эндометриальных белков, влияющих на имплантацию и раннее развитие эмбриона. Наиболее значимыми из них являются α-микроглобулин фертильности (АМГФ), α-микроглобулин беременности (АМГБ) — показатель активности маточных желез, а также плацентарный α-микроглобулин (ПАМГ — показатель децидуализации эндометрия). При Х.Э. сокращается выработка эндометрием иммуносупрессорных белков (АМГФ, ПАМГ). АМГФ вызывает увеличение продукции ИЛ-6 эпителием эндометрия, что дает возможность предполагать участие данного белка в формировании сети иммуномодулирующих пептидов, кроме того, известно его свойство подавлять активность естественных киллеров. Таким образом, вместо необходимого для успешного развития беременности Th-2 типа иммунного ответа наблюдается провоспалительный Th-1 тип [29].
У больных ХЭ обнаружены не только «стандартные» морфологические признаки ХЭ, но и высокий уровень экспрессии провоспалительного цитокина ФНО-α, факторов склероза и ангиогенеза (ТФР-β1, сосудистый эндотелиальный фактор роста), увеличение продукции индуктора апоптоза Bax, сдвиг соотношения Bcl-2/Bax в сторону активации программированной гибели клеток; снижение уровня экспрессии рецепторов прогестерона и эстрогенов. Все изложенные изменения были более выраженными в фолликулярную фазу и имели тенденцию к снижению в лютеиновую фазу менструального цикла [31].
Структурные и молекулярные перестройки эндометрия при ХЭ включают следующие факторы: нарушение созревания пиноподий к моменту «окна имплантации», наличие клеток воспалительного инфильтрата (лимфоцитов, плазмоцитов, макрофагов и др.), продуцирующих различные цитокины; фибробластические реакции и изменения в составе экстрацеллюлярного матрикса; снижение экспрессии LIF и повышение уровня апоптоза покровного и железистого эпителия функционального слоя [32].
Одним из важных аспектов патогенеза ХЭ является нарушение ангиоархитектоники эндометрия. В частности, обнаружены склерозирование стенок сосудов и образование периваскулярного склероза вокруг спиральных артерий и в базальных отделах эндометрия, что приводит к развитию его ишемии. Нарушение микроциркуляции, в свою очередь, приводит к повышению коагуляционного потенциала крови. Повреждение эндотелиальной поверхности сосудов служит одной из основных причин нарушения продукции и соотношения простациклина и тромбоксана, результатом чего являются тромбозы. Обсуждается вопрос о роли дисбаланса про- и антиоксидантной систем, а также влияния активных форм кислорода на развитие и прогрессирование хронического воспалительного процесса в эндометрии [33].
Таким образом, реализация хронического воспалительного процесса в эндометрии осуществляется на клеточном уровне в виде следующих нарушений: расстройства метаболизма, нарушения цепи иммунокомпетентной системы и развития аутоиммунных процессов, ухудшения микроциркуляции, нарастающей гипоксии, дисбаланса про- и антиоксидантной систем.
ХЭ является клинически значимой нозологической единицей с позиции репродуктологии, требуется дальнейшее изучение особенностей его этиологии и патогенеза с целью улучшения понимания течения воспалительного процесса и усовершенствования методов лечения и профилактики.