Найз и сирдалуд как принимать
Выбор фармакологической терапии при спастическом мышечном гипертонусе
Основными препаратами, используемыми для снижения мышечного тонуса, являются миорелаксанты. Рассмотрены вопросы выбора терапии с использованием антиспастических препаратов в зависимости от заболевания, выраженности мышечной спастичности, побочных эффектов
Myorelaxants are the basic preparations used for reduction in the muscular tone. Issues of selection of therapy by anti-spastic preparations depending on the disease, manifestation of muscular spasticity, side effects and special features of the preparation effect are considered.
Основными препаратами, используемыми для снижения мышечного тонуса, являются миорелаксанты. По механизму действия различают миорелаксанты центрального действия (влияют на синаптическую передачу возбуждения в центральной нервной системе) и периферического действия (угнетают прямую возбудимость поперечно-полосатых мышц). При применении миорелаксантов могут возникать достаточно значимые побочные действия, которые при выборе препарата надо тщательно оценивать [1, 2].
При выборе антиспастических препаратов учитывают в основном их способность тормозить полисинаптические рефлексы (уменьшение спастики), оказывая при этом наименьшее влияние на моносинаптические рефлексы (сила мышц). Антиспастический препарат должен уменьшать мышечную спастичность при минимальном снижении мышечной силы [3, 4].
Медикаментозная терапия основана на использовании таблетированных и инъекционных форм. Применяемые внутрь антиспастические средства, уменьшая мышечный тонус, могут улучшить двигательные функции, облегчить уход за обездвиженным пациентом, снять болезненные мышечные спазмы, усилить действие лечебной физкультуры, предупредить развитие контрактур [5]. При легкой степени спастичности применение миорелаксантов может привести к значительному положительному эффекту, однако при выраженной спастичности могут потребоваться большие дозы миорелаксантов, применение которых нередко вызывает нежелательные побочные эффекты. Лечение миорелаксантами начинают с минимальной дозы, затем ее медленно повышают для достижения эффекта [6].
К миoрелаксантам центрального действия, наиболее часто используемым в России для лечения спастического мышечного гипертонуса, относятся баклофен, тизанидин, толперизон, диазепам [7, 8].
Баклофен (Баклосан, Лиорезал) оказывает антиспастическое действие преимущественно на спинальном уровне. Препарат представляет аналог гамма-аминомасляной кислоты (ГАМК), который связывается с пресинаптическими ГАМК-рецепторами, приводя к уменьшению выделения возбуждающих аминокислот (глутамата, аспартата) и подавлению моно- и полисинаптической активности на спинальном уровне, что и вызывает снижение спастичности. Препарат проявляет также умеренное центральное анальгезирующее действие. Баклофен используется при спинальном и церебральном спастическом мышечном гипертонусе различного генеза. Начальная доза составляет 5–15 мг/сут (в один или три приема), затем дозу увеличивают на 5 мг каждый день до получения желаемого эффекта. Препарат принимают во время еды. Максимальная доза баклофена для взрослых составляет 60–75 мг/сут. Побочные эффекты чаще проявляются седацией, сонливостью, снижением концентрации внимания, головокружением и часто ослабевают в процессе лечения. Возможно возникновение тошноты, запоров и диареи, артериальной гипертонии, усиление атаксии, появление парестезий. Требуется осторожность при лечении больных пожилого возраста, пациентов, перенесших инсульт, пациентов с язвенной болезнью желудка и двенадцатиперстной кишки. Баклофен противопоказан при эпилепсии, наличии судорог в анамнезе [9, 10].
При выраженной спастичности, когда обычное пероральное применение антиспастических препаратов не эффективно, показано интратекальное введение баклофена, которое впервые было предложено в 1984 г. R. Penn. Для достижения необходимой концентрации препарата в спинномозговой жидкости необходимо принимать довольно значительные дозы баклофена, что может привести к нарушениям сознания, сонливости, слабости. В связи с этим были разработаны системы, при помощи которых баклофен доставляется непосредственно в подоболочечное пространство спинного мозга при помощи подоболочечной баклофеновой насосной системы. При этом клинического эффекта добиваются гораздо меньшими дозами баклофена, чем при использовании таблетированных форм [11, 12].
Данная система состоит из резервуара, где содержится баклофен или аналогичный препарат, насоса (помпы), при помощи которого препарат дозированно подается в подоболочечное пространство спинного мозга через люмбальный катетер и блока питания. Из резервуара баклофен поступает непосредственно в спинномозговую жидкость, а его дозировка контролируется специальным радиотелеметрическим устройством. Количество поступающего в спинномозговую жидкость лекарственного препарата можно изменять в зависимости от клинической картины. Добавление баклофена в резервуар производится через 2–3 месяца при помощи чрезкожной пункции [13].
Использование баклофеновой помпы улучшает скорость и качество ходьбы больных с нефиксированными рефлекторными контрактурами, обусловленными высокой спастичностью мышц-синергистов и дисбалансом мышц-антагонистов. Имеющийся 15-летний клинический опыт применения баклофена интратекально у больных, перенесших инсульт, свидетельствует о высокой эффективности этого метода в уменьшении не только степени спастичности, но и болевых синдромов и дистонических расстройств. Отмечено положительное влияние баклофеновой помпы на качество жизни больных, перенесших инсульт [14].
Тизанидин (Сирдалуд) — миорелаксант центрального действия, агонист альфа-2-адренергических рецепторов. Препарат снижает спастичность вследствие подавления полисинаптических рефлексов на уровне спинного мозга, что может быть вызвано угнетением высвобождения возбуждающих аминокислот L-глутамата и L-аспартата и активацией глицина, снижающего возбудимость интернейронов спинного мозга. Тизанидин обладает также умеренным центральным анальгетическим действием. Препарат эффективен при церебральной и спинальной спастичности, а также при болезненных мышечных спазмах. Начальная доза препарата составляет 2–6 мг/сут в один или три приема, при индивидуальном подборе увеличение дозы происходит на 3–4 день на 2 мг. При пероральном приеме действие препарата проявляется через 30–45 минут, максимальный эффект наступает в течение 1–2 часов. Средняя терапевтическая доза составляет 12–24 мг/сут, максимальная доза — 36 мг/сут. В качестве побочных эффектов могут возникнуть сонливость, сухость во рту, головокружение и снижение артериального давления, что ограничивает использование препарата при постинсультной спастичности. Антиспастический эффект тизанидина сопоставим с эффектом баклофена, однако тизанидин при адекватном подборе дозировки лучше переносится, т. к. не вызывает общей мышечной слабости и не усиливает мышечную слабость в парализованной конечности [15, 16].
Толперизон (Мидокалм) — антиспастический препарат центрального действия, угнетает каудальную часть ретикулярной формации и обладает Н-холинолитическими свойствами. Толперизон снижает активность спинальных нейронов, участвующих в формировании спастичности, путем ограничения потока натрия через мембрану нервных клеток. Наиболее часто используется по 300–450 мг/сут в два или три приема. Снижение мышечного тонуса при назначении толперизона иногда сопровождается сосудорасширяющим действием, что следует учитывать при назначении больным с тенденцией к артериальной гипотонии. Также препарат может вызывать или усиливать у больных недержание мочи [17].
Основным побочным эффектом баклофена, тизанидина и толперизона является быстрое наступление мышечной слабости, причем в каждом случае врач должен находить баланс между снижением тонуса и усилением слабости. Кривая баланса между снижением спастического тонуса и усилением мышечной слабости у больных на фоне увеличения дозы Мидокалма, Сирдалуда или Баклофена показывает, что наиболее быстрое усиление слабости происходит при приеме Баклофена, а самый мягкий препарат, позволяющий эффективно подобрать индивидуальную дозировку, — Мидокалм. Во всех случаях, учитывая наличие узкого терапевтического окна, курс лечения начинают с небольшой дозы препарата, постепенно наращивая ее до достижения отчетливого антиспастического эффекта, но не до появления слабости [18, 19].
Диазепам (Реаланиум, Релиум, Сибазон) является миорелаксантом, поскольку обладает способностью стимулировать уменьшенное пресинаптическое торможение на спинальном уровне. Он не имеет прямых ГАМК-ергических свойств, увеличивает концентрацию ацетилхолина в мозге и тормозит обратный захват норадреналина и дофамина в синапсах. Это приводит к усилению пресинаптического торможения и проявляется снижением сопротивляемости растяжению, увеличением диапазона движений. Диазепам также обладает способностью уменьшать болевой синдром, вызываемый спазмом мышц. Наряду со снижением мышечного тонуса, развиваются заторможенность, головокружение, нарушение внимания и координации ввиду токсического действия на центральную нервную систему. Это значительно ограничивает применение диазепама в качестве миорелаксанта. Используется он, в основном, для лечения спастичности спинального происхождения при необходимости кратковременного снижения мышечного тонуса. Для лечения спастичности назначают в дозе 5 мг однократно или по 2 мг 2 раза в день. Максимальная суточная доза может составлять 60 мг. При больших дозах могут отмечаться расстройства сознания, преходящая дисфункция печени и изменения крови. Продолжительность лечения ограничена из-за возможного развития лекарственной зависимости [20].
Клоназепам является производным бензодиазепина. Клоназепам оказывает успокаивающее, центральное миорелаксирующее, анксиолитическое действие. Миорелаксирующий эффект достигается за счет усиления ингибирующего действия ГАМК на передачу нервных импульсов, стимуляции бензодиазепиновых рецепторов, расположенных в аллостерическом центре постсинаптических ГАМК-рецепторов восходящей активирующей ретикулярной формации ствола головного мозга и вставочных нейронов боковых рогов спинного мозга, а также уменьшения возбудимости подкорковых структур головного мозга и торможения полисинаптических спинальных рефлексов.
Быстрое наступление сонливости, головокружения и привыкания ограничивает применение этого препарата. Для снижения проявления возможных побочных реакций, достигать терапевтической дозы необходимо путем медленного титрования в течение двух недель. Для приема внутрь взрослым рекомендуется начальная доза не более 1 мг/сут. Поддерживающая доза — 4–8 мг/сут. Возможно назначение небольших доз в сочетании с другими миорелаксантами. Клоназепам эффективен при пароксизмальных повышениях мышечного тонуса. Противопоказан при острых заболеваниях печени, почек, миастении [21].
Дикалия клоразепат (Транксен) — аналог бензодиазепина, трансформируется в главный метаболит диазепама, обладает большей активностью и длительностью антиспастического действия, чем диазепам. Отмечен его хороший эффект при лечении в виде уменьшения фазических рефлексов на растяжение, обладает незначительным седативным эффектом. Первоначальная доза составляет 5 мг 4 раза в сутки, затем уменьшается до 5 мг 2 раза в сутки [22].
Дантролен — производное имидазолина, действует вне центральной нервной системы, преимущественно на уровне мышечных волокон. Механизм действия дантролена — блокирование высвобождения кальция из саркоплазматического ретикулума, что ведет к снижению степени сократимости скелетных мышц, редукции мышечного тонуса и фазических рефлексов, увеличению диапазона пассивных движений. Важным преимуществом дантролена по отношению к другим миорелаксантам является его доказанная эффективность в отношении спастичности не только спинального, но и церебрального генеза. Начальная доза — 25 мг/сут, при переносимости дозу увеличивают в течение 4 недель до 400 мг/сут. Побочные эффекты — сонливость, головокружение, тошнота, диарея, снижение скорости клубочковой фильтрации. Серьезную опасность, особенно у пожилых пациентов в дозе более 200 мг/сут, представляет гепатотоксическое действие, поэтому в период лечения надо регулярно следить за функцией печени. Элиминация дантролена на 50% осуществляется за счет печеночного метаболизма, в связи с этим он противопоказан при заболеваниях печени. Осторожность следует соблюдать и при тяжелых сердечных или легочных заболеваниях.
Катапресан — применяется в основном при спинальных повреждениях, действует на альфа-2-агонисты головного мозга, обладает пресинаптическим торможением. Из побочных эффектов отмечаются снижение артериального давления и депрессия. Первоночальная доза — 0,05 мг 2 раза в день, максимальная — 0,1 мг 4 раза в день.
Темазепам — взаимодействует с бензодиазепиновыми рецепторами аллостерического центра постсинаптических ГАМК-рецепторов, расположенных в лимбической системе, восходящей активирующей ретикулярной формации, гиппокампе, вставочных нейронах боковых рогов спинного мозга. В результате открываются каналы для входящих токов ионов хлора и таким образом потенцируется действие эндогенного тормозного медиатора — ГАМК. Рекомендуемая доза — 10 мг 3 раза в день. Эффективно его сочетание с баклофеном [23, 24].
Основные лекарственные средства, используемые для лечения спастического мышечного гипертонуса, представлены в табл.
Таким образом, выбор препарата определяется основным заболеванием, выраженностью мышечной спастичности, а также побочными эффектами и особенностями действия конкретного препарата.
Так, например, тизанидин и баклофен в большей степени действуют на тонус мышц-разгибателей, поэтому в случаях наличия значительного гипертонуса мышц-сгибателей руки, легкой спастичности мышц ноги их прием не показан, поскольку легкое повышение тонуса мышц-разгибателей ноги компенсирует мышечную слабость в ноге и стабилизирует походку больного. В таком случае средством выбора являются методы физического воздействия на мышцы верхней конечности.
При лечении церебральной спастичности наиболее часто применяют Сирдалуд, а при спинальной спастичности — Сирдалуд и Баклофен. Важным преимуществом перед другими миорелаксантами обладает Мидокалм, который не оказывает седативного эффекта и имеет благоприятный спектр переносимости, поэтому является препаратом выбора для лечения в амбулаторных условиях и для лечения пожилого контингента пациентов.
Допустима комбинация нескольких средств, что позволяет эффективно снижать тонус на меньших дозах каждого из препаратов. Сочетание препаратов с разными точками приложения, начиная от центров в головном мозге и до мышц, может привести к суммированию терапевтического эффекта.
Эффективность пероральных антиспастических препаратов снижается при их длительном использовании, часто возникает необходимость возрастающего повышения дозировок для поддержания начального клинического эффекта, что сопровождается увеличением частоты и тяжести побочных реакций [25–27].
В ситуации, когда спастичность носит локальный характер и системный эффект пероральных миорелаксантов нежелателен, предпочтительны локальные методы воздействия, одним из которых является локальное введение ботулотоксина [28, 29].
Литература
А. А. Королев, кандидат медицинских наук
ФГБУ «Всероссийский центр экстренной и радиационной медицины им. А. М. Никифорова» МЧС России, Санкт-Петербург
Подходы к лечению боли с учетом механизмов ее развития
Г.Р. Имаметдинова, Н.В. Чичасова, Е.В. Иголкина
ГБОУ ВПО «Первый МГМУ им. И.М. Сеченова» Минздрава России, Москва
Рассмотрены проблемы лечения острой и хронической боли у больных с ревматическими заболеваниями. Показана роль воспаления и мышечного спазма в патогенезе острой и хронической боли. Представлены результаты клинических исследований и использования в клинической практике нимесулида (Найз ® ) и тизанидина (Сирдалуд ® ) при лечении острой и хронической боли.
Ключевые слова: боль, воспаление, мышечный спазм, нимесулид (Найз ® ), тизанидин (Сирдалуд ® ).
Approaches to treating pain in terms of the mechanisms of its development G.R.
Imametdinova, N.V. Chichasova, E.V. Igolkina
I.M. Sechenov First Moscow State Medical University, Ministry of Health of Russia, Moscow
The paper considers problems in the treatment of acute and chronic pain in patients with rheumatic diseases and shows the role of inflammation and muscle spasm in the pathogenesis of acute and chronic pain. It gives the results of clinical trials and the clinical use of nimesulide (Nise ® ) and tizanidine (Sirdalud ® ) in the treatment of acute and chronic pain.
Key words: pain, inflammation, muscle spasm, nimesulide (Nise ® ), tizanidine (Sirdalud ® ).
Самой распространенной причиной, заставляющей пациента обратиться к врачу, является боль. Боль сопровождает около 70% всех известных заболеваний. Распространенность хронической боли в популяции колеблется от 2 до 49% [1]. Наиболее часто боль возникает в различных структурах опорно-двигательного аппарата и является одним из основных симптомов ревматических заболеваний (РЗ), к которым относят воспалительные, дегенеративные заболевания суставов, позвоночника и периартикулярных тканей. В различные периоды жизни боль в связи с поражением компонентов опорно-двигательного аппарата встречается хотя бы 1 раз у 20-45% населения земного шара, чаще у женщин, чем у мужчин, и чаще в старших возрастных группах [2, 3].
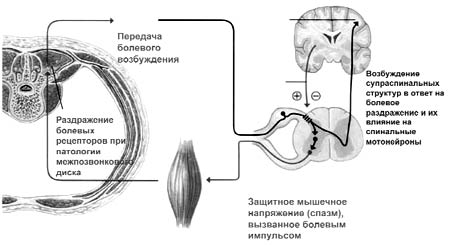
Рис. 1. Механизм развития порочного круга
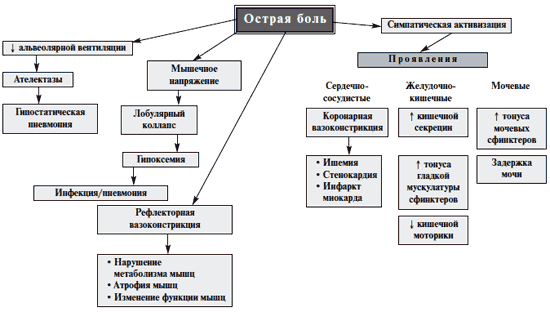
Боль является значимой медицинской проблемой. Острая и хроническая боль может приводить к функциональным нарушениям сердечно-сосудистой, дыхательной, пищеварительной, мочевыделительной систем 11 (рис. 2). Возникнув вследствие того или иного повреждения, боль приводит к серьезным нарушениям в системе регуляции болевой чувствительности, вызывает психологические расстройства, формирует у пациента особый тип болевого поведения [14].
Рис. 2. Висцеральные эффекты острой боли
Боль в структурах опорно-двигательного аппарата требует комплексного фармакологического подхода. Расширение представлений о генезе боли обусловливают новые подходы к проводимой терапии. Медикаментозная терапия включает использование нестероидных противовоспалительных препаратов (НПВП) и вспомогательных анальгетических средств (миорелаксанты) [4].
НПВП относятся к числу наиболее широко применяемых в клинической практике лекарственных средств. Основными показаниями к их назначению являются воспалительные процессы различного генеза, боль, лихорадка, необходимость профилактики тромбозов [15].
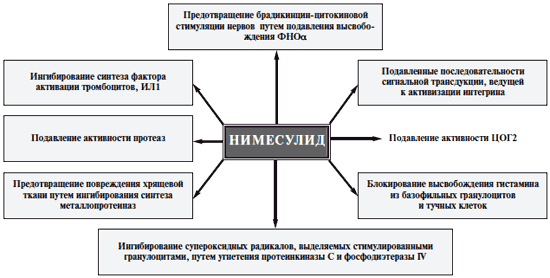
Таким требованиям соответствует селективный ингибитор ЦОГ2 нимесулид. Он является одним из наиболее широко используемых в России препаратов группы селективных НПВП. По анальгетическому, противовоспалительному и жаропонижающему действию нимесулид не уступает неселективным НПВП, а по некоторым данным, даже несколько их превосходит [20].
Рис. 3. Механизмы действия нимесулида
Нимесулид относится к короткоживущим НПВП. Период полувыведения составляет от 1,8 до 4,7 ч, что способствует снижению частоты побочных эффектов препарата. При пероральном приеме нимесулид быстро и практически полностью абсорбируется независимо от приема пищи. Нимесулид отличается быстрым достижением максимальной концентрации. Уже через 30 мин после перорального приема концентрация препарата в плазме крови и синовиальной жидкости достигает 25-80% от максимальной, что обусловливает высокую скорость наступления анальгетического эффекта. Благодаря биохимическим свойствам нимесулид легко попадает в очаг воспаления. Концентрация свободного нимесулида непосредственно в очаге воспаления (особенно в ткани сустава), где рН среды более низкий, может быть намного выше, чем его плазменная концентрация [33, 34]. Препарат выводится с мочой и калом.
По данным мировой литературы, частота побочных явлений при лечении нимесулидом колеблется в пределах 6,8-36% с четкой зависимостью от дозы и длительности приема препарата. В частности, при анализе результатов нескольких клинических испытаний, включавших 22 938 больных ОА, леченных нимесулидом в дозе 100-400 мг в течение 5-21 дня (в среднем 12 дней), общая частота побочных реакций составила 8,2% [34]. В другом многоцентровом исследовании, в котором участвовало 12 607 пациентов с различными РЗ и ортопедическими заболеваниями, на фоне лечения нимесулидом 400-200 мг/сут в течение 21 дня частота развития побочных эффектов составила 6,8%. При специальном анализе вошедших в эти 2 исследования 8354 пациентов старше 60 лет оказалось, что частота побочных эффектов равнялась 8,9% и не отличалась от таковой в общей популяции больных [35].
По данным отечественных и зарубежных авторов, нимесулид крайне редко вызывает усиление бронхоспазма у больных, страдающих бронхиальной астмой и гиперчувствительностью к ацетилсалициловой кислоте или другим НПВП, так как не обладает перекрестной реактивностью с этой кислотой и неселективными НПВП в отношении индукции обострения астмы и является одним из препаратов выбора (среди селективных НПВП) для этих больных [25, 36].
Отличительной особенностью нимесулида является отсутствие отрицательного действия на хрящ, что обусловлено механизмом его действия: способностью влиять на апоптоз хондроцитов [28], ингибировать ИЛ 1|3 в культуре синовиальных фибробластов [27] и металлопротеаз. Это дает возможность применять его у пациентов с ОА.
Результаты многочисленных исследований, выполненных отечественными и зарубежными авторами, подтверждают высокую эффективность нимесулида при лечении как острой, так и хронической боли. Высокая анальгетическая эффективность нимесулида показана при острых травмах, после хирургических вмешательств, при острой боли в нижней части спины [37, 38], а также при заболеваниях опорно-двигательного аппарата, головной боли, дисменорее. По анальгетической активности нимесулид не уступает индометацину, диклофенаку, пироксикаму [39].
Более быстрый и выраженный эффект нимесулида по сравнению с диклофенаком был продемонстрирован при купировании острого подагрического артрита и поражении периартикулярных тканей [37, 40].
Результаты работ отечественных исследователей, посвященных применению нимесулида у больных ОА, указывают на его высокую эффективность и хорошую переносимость при отсутствии отрицательного влияния на хрящ.
Как свидетельствуют многочисленные исследования, нимесулид характеризуется высокой гастроэнтерологической безопасностью [3]. Весьма интересным является тот факт, что низкую частоту поражения ЖКТ на фоне лечения нимесулидом связывают не только с ЦОГ2-селективностью препарата, но и с антигистаминным действием, приводящим к снижению секреции соляной кислоты в желудке [41].
Следует отметить, что пациенты, страдающие ОА, подвержены высокому риску развития ЖКТ-осложнений в связи с возрастом, частым развитием сосудистой, кардиальной, ренальной патологии и необходимостью прибегать к сопутствующей терапии. Нимесулид (Найз ® ) использовался у этой категории больных в суточной дозе 200 мг, что обеспечивало достижение клинического эффекта у 87-93% больных [47, 48] при хорошей переносимости в отношении ЖКТ Это подтверждено и данными зарубежных контролируемых исследований [49, 50], а также постмаркетингового изучения переносимости нимесулида в 17 странах у 11 831 385 больных [35, 51].
В течение 6 мес проводилось сравнительное исследование эффективности и переносимости нимесулида в суточной дозе 200 мг и диклофенака в суточной дозе 150 мг у 279 больных ОА. Эффективность обоих препаратов была сопоставимой при лучшей переносимости нимесулида: развитие побочных реакций со стороны ЖКТ было зафиксировано у 36 и 47% пациентов соответственно (р ® ) у больных ОА с артериальной гипертензией (АГ) показало отсутствие у него негативного влияния на течение АГ как по уровню среднесуточного артериального давления (АД), так и по потребности в антигипертензивной терапии [53]. Аналогичные результаты продемонстрированы в исследовании, включавшем 40 больных РА, которые получали нимесулид (Найз ® ) в течение 6 мес. По результатам суточного мониторинга не отмечено негативного влияния на АД, а также отсутствовала иная отрицательная динамика со стороны сердечно-сосудистой системы, что было подтверждено ЭКГ-мониторингом и эхокардиографией [54]. По данным анализа, проведенного A. Helin-Salmivaara и соавт., значение относительного риска инфаркта миокарда для нимесулида составило 1,69, что было сопоставимо с аналогичным показателем для мелоксикама, набуметона и неселективных НПВП [55].
Данные, полученные в результате метаанализа, показали, что нимесулид не вызывает побочные реакции со стороны почек. Оказалось, что на 100 тыс. пациентов, принимавших нимесулид, за 10 лет отмечено только 11 случаев возможной связи почечных осложнений с приемом препарата, из которых только в четырех проводилась монотерапия нимесулидом [57, 58].
Анализ данных литературы указывает на то, что гепатотоксичность нимесулида не выше, чем у многих других представителей класса НПВП [59]. Так, при назначении нимесулида коротким курсом (не более 30 дней) повышение уровня АЛТ и АСТ в 2 раза и более отмечается лишь у 0,4% больных, а при длительном многомесячном приеме частота подобных изменений не превышает 1,5% [60, 61]. В исследовании G. Traversa и соавт. частота серьезных осложнений со стороны печени при использовании нимесулида составила 35,3 на 100 тыс. человеко-лет, что меньше в сравнении с диклофенаком (39,2), кеторолаком (66,8), ибупрофеном (44,6) [62].
Особый интерес представляет работа отечественных авторов, посвященная изучению влияния нимесулида на функцию печени при лечении подагрического артрита. Как известно, для пациентов с подагрой часто характерны метаболические нарушения и высокая частота злоупотребления алкоголем, что способствует развитию побочных реакций со стороны печени. На фоне использования нимесулида в суточной дозе от 100 до 400 мг отсутствовала отрицательная динамика биохимических показателей крови, свидетельствующих о поражении печеночных клеток или холестазе [63].
Таким образом, быстрота развития и выраженность анальгетического, противовоспалительного эффекта в сочетании с хорошей переносимостью позволяют использовать нимесулид при лечении острой и хронической боли и определяют возможность его применения в течение длительного времени.
Между тем в ряде случаев применение НПВП не дает оптимального анальгетического эффекта. Одной из причин этого может служить наличие стойкого мышечного спазма в области поражения [64].
Дополнительными препаратами для лечения острой и хронической боли при заболеваниях опорно-двигательного аппарата являются центральные миорелаксанты. Эти препараты устраняют мышечный спазм как один из важных компонентов боли или уменьшают его выраженность. Применение миорелаксантов способствует облегчению боли, предотвращению образования контрактур, улучшению функциональной способности опорно-двигательного аппарата [65].
Одним из наиболее эффективных современных миорелаксантов является тизанидин (Сирдалуд ® ). Тизанидин относится к миорелаксантам центрального действия (α2-адренергическим агонистам) и реализует свой эффект на спинальном и супраспинальном уровнях. Стимулируя пресинаптические α2-рецепторы, он подавляет высвобождение возбуждающих аминокислот, которые стимулируют НМДА-рецепторы. Это приводит к угнетению полисинаптических рефлексов головного мозга, ответственных за гипертонус мышц, и подавлению передачи возбуждения через них, что вызывает снижение повышенного тонуса и ослабление болезненных мышечных спазмов. В дополнение к миорелаксирующим свойствам тизанидин дает центральный анальгетический эффект (за счет снижения высвобождения возбуждающих нейромедиаторов в головном мозге) [66, 67].
При пероральном приеме препарат быстро и практически полностью абсорбируется. Максимальная концентрация в плазме крови достигается через 1-2 ч. Период полувыведения составляет 3-5 ч. Прием пищи не влияет на фармакокинетику препарата. С белками плазмы крови тизанидин связывается не более чем на 30%. Экскреция препарата и его метаболитов осуществляется с мочой [68].
Установлено, что Сирдалуд ® хорошо переносится. Как при краткосрочном, так и при длительном применении малых доз препарата, к которым обычно прибегают в ревматологии, нежелательные явления возникают редко и купируются при отмене препарата [69]. Побочные реакции со стороны сердечно-сосудистой системы при использовании тизанидина в дозах, вызывающих миорелаксирующий эффект, выражены слабо и носят преходящий характер [69]. Наиболее частыми побочными эффектами являются сонливость, заторможенность (пациентам следует рекомендовать воздержаться от видов работ, требующих концентрации внимания и быстрой реакции), головокружение, сухость во рту. Препарат дает гипотензивный эффект, который значительно усиливается при одновременном применении с сильными ингибиторами CYP1A2, такими как некоторые антиаритмические препараты, фторхинолоны. Необходимо принимать во внимание, что при сочетанном применении тизанидина с антигипертензивными препаратами и диуретиками возможны выраженная гипотония и брадикардия, поэтому одновременное использование тизанидина с этими препаратами не рекомендуется. Повышение уровня печеночных трансаминаз наблюдается редко [66, 68].
Список использованной литературы
_575.gif)