Мышьяк как обозначается в химии
Мышьяк
Мышьяк / Arsenicum (As), 33
[Ar] 3d 10 4s 2 4p 3
2,18 [1] (шкала Полинга)
5,73 (серый мышьяк) г/см³
1090 К (817°C), 3700 кПа
Мышья́к — химический элемент 15-й группы (по устаревшей классификации — главной подгруппы пятой группы) четвёртого периода периодической системы; имеет атомный номер 33, обозначается символом As. Простое вещество представляет собой хрупкий полуметалл стального цвета. CAS-номер: 7440-38-2.
Содержание
История
Происхождение названия
В 1789 году А. Л. Лавуазье выделил металлический мышьяк из триоксида мышьяка («белого мышьяка»), обосновал, что это самостоятельное простое вещество, и присвоил элементу название «арсеникум».
Нахождение в природе
Месторождения
Получение
Открытие способа получения металлического мышьяка (серого мышьяка) приписывают средневековому алхимику Альберту Великому, жившему в XIII в. Однако гораздо ранее греческие и арабские алхимики умели получать мышьяк в свободном виде, нагревая «белый мышьяк» (триоксид мышьяка) с различными органическими веществами.
Существует множество способов получения мышьяка: сублимацией природного мышьяка, способом термического разложения мышьякового колчедана, восстановлением мышьяковистого ангидрида и др.
В настоящее время для получения металлического мышьяка чаще всего нагревают арсенопирит в муфельных печах без доступа воздуха. При этом освобождается мышьяк, пары которого конденсируются и превращаются в твердый мышьяк в железных трубках, идущих от печей, и в особых керамических приёмниках. Остаток в печах потом нагревают при доступе воздуха, и тогда мышьяк превращается в As2O3. Металлический мышьяк получается в довольно незначительных количествах, и главная часть мышьякосодержащих руд перерабатывается в белый мышьяк, то есть в триоксид мышьяка — мышьяковистый ангидрид As2О3.
Применение
Мышьяк используется для легирования сплавов свинца, идущих на приготовление дроби, так как при отливке дроби башенным способом капли сплава мышьяка со свинцом приобретают строго сферическую форму, и кроме того, прочность и твёрдость свинца возрастают.
Мышьяк особой чистоты (99,9999 %) используется для синтеза ряда ценных и важных полупроводниковых материалов — арсенидов и сложных алмазоподобных полупроводников.
Сульфидные соединения мышьяка — аурипигмент и реальгар — используются в живописи в качестве красок и в кожевенной отрасли промышленности в качестве средств для удаления волос с кожи.
В пиротехнике реальгар употребляется для получения «греческого», или «индийского», огня, возникающего при горении смеси реальгара с серой и селитрой (ярко-белое пламя).
Многие из мышьяковых соединений в очень малых дозах применяются в качестве лекарств для борьбы с малокровием и рядом тяжелых заболеваний, так как оказывают клинически значимое стимулирующее влияние на ряд функций организма, в частности, на кроветворение. Из неорганических соединений мышьяка мышьяковистый ангидрид может применяться в медицине для приготовления пилюль и в зубоврачебной практике в виде пасты как некротизирующее лекарственное средство. Этот препарат называли «мышьяк» и применялся в стоматологии для девитализации пульпы зуба (см. пульпит). В настоящее время препараты мышьяка применяются в зубоврачебной практике редко из-за токсичности. Разработаны и применяются другие методы безболезненной денервации зуба под местной анестезией.
Биологическая роль и физиологическое действие
Мышьяк и все его соединения ядовиты. При остром отравлении мышьяком наблюдаются рвота, боли в животе, понос, угнетение центральной нервной системы. Сходство симптомов отравления мышьяком с симптомами холеры длительное время позволяло маскировать использование соединений мышьяка (чаще всего, триоксида мышьяка) в качестве смертельного яда. Во Франции порошок триоксида мышьяка за высокую «эффективность» получил обиходное название «наследственный порошок» (фр. poudre de succession ). Существует предположение, что соединениями мышьяка был отравлен Наполеон на острове Святой Елены. В 1832 году появилась надёжная качественная реакция на мышьяк — проба Марша, значительно повысившая эффективность диагностирования отравлений.
На территориях, где в почве и воде избыток мышьяка, он накапливается в щитовидной железе у людей и вызывает эндемический зоб.
Помощь и противоядия при отравлении мышьяком: приём водных растворов тиосульфата натрия Na2S2O3, промывание желудка, приём молока и творога; специфическое противоядие — унитиол. ПДК в воздухе для мышьяка 0,5мг/м³.
Работают с мышьяком в герметичных боксах, используя защитную спецодежду. Из-за высокой токсичности соединения мышьяка использовались как отравляющие вещества в Первую мировую войну.
Мышьяк в малых дозах канцерогенен, его использование в качестве лекарства, «улучшающего кровь» (так называемый «белый мышьяк», например «Таблетки Бло с мышьяком», и др.) продолжалось до середины 1950-х гг., и внесло свой весомый вклад в развитие онкологических заболеваний.
Недавно широкую огласку получила техногенная экологическая катастрофа на юге Индии — из-за чрезмерного отбора воды из водоносных горизонтов мышьяк стал поступать в питьевую воду. Это вызвало токсическое и онкологическое поражение у десятков тысяч людей.
Считалось также, что «При длительном потреблении небольших доз мышьяка у организма вырабатывается иммунитет: Этот факт установлен как для людей, так и для животных. Известны случаи, когда привычные потребители мышьяка принимали сразу дозы, в несколько раз превышающие смертельную, и оставались здоровыми. Опыты на животных показали своеобразие этой привычки. Оказалось, что животное, привыкшее к мышьяку при его употреблении, быстро погибает, если значительно меньшая доза вводится в кровь или под кожу.» Однако такое «привыкание» носит очень ограниченный характер, в отношении т. н. «острой токсичности», и не защищает от новообразований. Тем не менее, в настоящее время исследуется влияние микродоз мышьяксодержащих препаратов в качестве противоракового средства.
Загрязнения мышьяком
Мышьяк

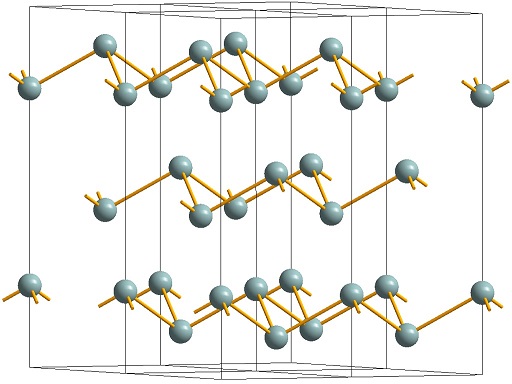
СТРУКТУРА
СВОЙСТВА
МОРФОЛОГИЯ

ПРОИСХОЖДЕНИЕ

В литературе имеются указания на вторичное происхождение мышьяка в зонах выветривания месторождений мышьяковистых руд, что, вообще говоря, мало вероятно, если учесть, что в этих условиях он очень неустойчив и, быстро окисляясь, разлагается полностью. Черные корочки состоят из тонкой смеси мышьяка и арсенолита (As2О3). В конце концов образуется чистый арсенолит.
В земной коре концентрация мышьяка невелика и составляет 1,5 промилле. Он встречается в почве и минералах и может попасть в воздух, воду и грунт благодаря ветровой и водной эрозии. Кроме того, элемент поступает в атмосферу из других источников. В результате извержения вулканов в воздух выделяется около 3 тыс. т мышьяка в год, микроорганизмы образуют 20 тыс. т летучего метиларсина в год, а в результате сжигания ископаемого топлива за тот же период выделяется 80 тыс. т.
На территории СССР самородный мышьяк был встречен в нескольких месторождениях. Из них отметим Садонское гидротермальное свинцово-цинковое месторождение, где он неоднократно наблюдался в виде почковидных масс на кристаллическом кальците с галенитом и сфалеритом. Крупные почкообразные скопления самородного мышьяка с концентрически-скорлуповатым строением были встречены на левом берегу р. Чикоя (Забайкалье). В парагенезисе с ним наблюдался лишь кальцит в виде оторочек на стенках тонких жил, секущих древние кристаллические сланцы. В виде обломков (рис. 76) мышьяк был найден также в районе ст. Джалинда, Амурской ж. д. и в других местах.
В ряде месторождений Саксонии (Фрейберг, Шнееберг, Аннаберг и др.) самородный мышьяк наблюдался в ассоциации с мышьяковистыми соединениями кобальта, никеля, серебра, самородным висмутом и др. Все эти и другие находки этого минерала практического значения не имеют.
ПРИМЕНЕНИЕ

Сульфидные соединения мышьяка — аурипигмент и реальгар — используются в живописи в качестве красок и в кожевенной отрасли промышленности в качестве средств для удаления волос с кожи. В пиротехнике реальгар употребляется для получения «греческого», или «индийского», огня, возникающего при горении смеси реальгара с серой и селитрой (при горении образует ярко-белое пламя).
Некоторые элементоорганические соединения мышьяка являются боевыми отравляющими веществами, например, люизит.
В начале XX века некоторые производные какодила, например, сальварсан, применяли для лечения сифилиса, со временем эти препараты были вытеснены из медицинского применения для лечения сифилиса другими, менее токсичными и более эффективными, фармацевтическими препаратами, не содержащими мышьяк.
Многие из мышьяковых соединений в очень малых дозах применяются в качестве препаратов для борьбы с малокровием и рядом других тяжелых заболеваний, так как оказывают клинически заметное стимулирующее влияние на ряд специфических функций организма, в частности, на кроветворение. Из неорганических соединений мышьяка мышьяковистый ангидрид может применяться в медицине для приготовления пилюль и в зубоврачебной практике в виде пасты как некротизирующее лекарственное средство. Этот препарат в обиходе и жаргонно называли «мышьяк» и применяли в стоматологии для локального омертвления зубного нерва. В настоящее время препараты мышьяка редко применяются в зубоврачебной практике из-за их токсичности. Сейчас разработаны и применяются другие методы безболезненного омертвления нерва зуба под местной анестезией.
Мышьяк
| Мышьяк(As) | |
|---|---|
| Атомный номер | 33 |
| Внешний вид | хрупкий полуметалл стального цвета |
| Свойства атома | |
| Атомная масса (молярная масса) | 74,92159 а. е. м. (г/моль) |
| Радиус атома | 139 пм |
| Энергия ионизации (первый электрон) | 946,2(9,81) кДж/моль (эВ) |
| Электронная конфигурация | [Ar] 3d 10 4s 2 4p 3 |
| Химические свойства | |
| Ковалентный радиус | 120 пм |
| Радиус иона | (+5e)46 (-3e)222 пм |
| Электроотрицательность (по Полингу) | 2,18 |
| Электродный потенциал | 0 |
| Степени окисления | 5, 3, −2 |
| Термодинамические свойства | |
| Плотность | 5,73 (grey arsenic) г/см³ |
| Удельная теплоёмкость | 0,328 Дж/(K·моль) |
| Теплопроводность | (50,2) Вт/(м·K) |
| Температура плавления | 1090 K |
| Теплота плавления | n/a кДж/моль |
| Температура кипения | 876 K |
| Теплота испарения | 32,4 кДж/моль |
| Молярный объём | 13,1 см³/моль |
| Кристаллическая решётка | |
| Структура решётки | тригональная |
| Период решётки | 4,130 Å |
| Отношение c/a | 2,805 |
| Температура Дебая | 285,00 K |
Содержание
История
Мышьяк известен человечеству с древнейших времен, когда использовались в качестве красителей минералы аурипигмент As2S3 и реальгар As4S4 (упоминания о них встречаются у Аристотеля).
Алхимики при прокаливании сульфидов мышьяка на воздухе отмечали, что образование так называемого белого оксида As2O3:
Впервые мышьяк в свободном виде получил немецкий алхимик А. фон Больдштндт в 13 веке прогреванием оксида мышьяка с углем:
Для изображения мышьяка использовали знак извивающейся змеи с раскрытой пастью.
Происхождение названия
Нахождение в природе
Получение
Физические и химические свойства
Расплавить мышьяк можно только в запаянных ампулах под давлением. Температура плавления 817 °C при давлении его насыщенных паров 3,6 МПа. Структура серого мышьяка похожа на структуру серой сурьмы и по строению напоминает черный фосфор.
Мышьяк химически активен. При хранении на воздухе порошкообразный мышьяк воспламеняется с образованием кислотного оксида As2O3. Этот оксид в парах существует в виде димеров As4O6.
При осторожном обезвоживании мышьяковой кислоты H3AsO4 получают высший кислотный оксид мышьяка As2O5, который при нагревании легко отдает кислород, превращаясь в As2O3.
Оксиду As2O3 отвечают существующие только в растворах слабые кислоты — ортомышьяковистая H3AsO3 и метамышьяковистая HAsO2. Их соли — арсенаты.
Разбавленная азотная кислота окисляет мышьяк до H3AsO3, концентрированная азотная кислота — до H3AsO4. Со щелочами мышьяк не реагирует, в воде растворяется.
При нагревании мышьяка и водорода образуется арсин AsH3 — очень токсичный газ с запахом чеснока. С фтором и хлором мышьяк взаимодействует с самовоспламенением. При взаимодействии мышьяка с серой, селеном и теллуром образуются халькогениды : As2S5, As2S3, As4S4, As2Se3, As2Te3, существующие в стеклообразном состоянии. Они являются полупроводниками.
Известно большое число органических соединений мышьяка, в которых имеется химическая связь As — C: органоарсины RnAsH3-n (n = 1,3), тетраорганодиарсины R2As — AsR2 и другие.
Применение
Мышьяк используется для легирования сплавов свинца, идущих на приготовление дроби, так как при отливке дроби башенным способом капли сплава мышьяка со свинцом приобретают строго сферическую форму, и кроме того, прочность и твёрдость свинца возрастают. Мышьяк особой чистоты используется для синтеза ряда практически очень ценных и важных полупроводниковых материалов — арсенидов и сложных алмазоподобных полупроводников.
Биологическая роль и физиологическое действие
Недавно широкую огласку получила техногенная экологическая катастрофа на юге Индии — из-за повышенного отбора воды из водоносных горизонтов, мышьяк стал поступать в питьевую воду. Это вызвало токсическое и онкологическое поражение у десятков тысяч людей.
Считалось также, что «При длительном потреблении небольших доз мышьяка у организма вырабатывается иммунитет: Этот факт установлен как для людей, так и для животных. Известны случаи, когда привычные потребители мышьяка принимали сразу дозы, в несколько раз превышающие смертельную, и оставались здоровыми. Опыты на животных показали своеобразие этой привычки. Оказалось, что животное, привыкшее к мышьяку при его употреблении, быстро погибает, если значительно меньшая доза вводится в кровь или под кожу.» Однако такое «привыкание» носит очень ограниченный характер, в отношении т. н. «острой токсичности», и не защищает от новообразований. Тем не менее, в настоящее время исследуется влияние микродоз мышьяксодержащих препаратов в качестве противоракового средства.
Глоссарий. Химия
Мышья́к — химический элемент с атомным номером 33 в периодической системе химических элементов Д.И. Менделеева, обозначается символом As. Представляет собой хрупкий полуметалл стального цвета.
Происхождение названия
Название мышьяка в русском языке связывают с употреблением его соединений для истребления мышей и крыс. Греческое название ἀρσενικόν происходит от персидского زرنيخ (zarnik) — «жёлтый аурипигмент». Народная этимология возводит к др.-греч. ἀρσενικός — мужской. В 1789 году А. Л. Лавуазье выделил металлический мышьяк из триоксида мышьяка («белого мышьяка»), обосновал, что это самостоятельное простое вещество, и присвоил элементу название «арсеникум».
Получение
Открытие способа получения металлического мышьяка (серого мышьяка) приписывают средневековому алхимику Альберту Великому, жившему в XIII в. Однако гораздо ранее греческие и арабские алхимики умели получать мышьяк в свободном виде, нагревая «белый мышьяк» (триоксид мышьяка) с различными органическими веществами. Существует множество способов получения мышьяка: сублимацией природного мышьяка, способом термического разложения мышьякового колчедана, восстановлением мышьяковистого ангидрида и др. В настоящее время для получения металлического мышьяка чаще всего нагревают арсенопирит в муфельных печах без доступа воздуха. При этом освобождается мышьяк, пары которого конденсируются и превращаются в твердый мышьяк в железных трубках, идущих от печей, и в особых керамических приёмниках. Остаток в печах потом нагревают при доступе воздуха, и тогда мышьяк превращается в As2O3. Металлический мышьяк получается в довольно незначительных количествах, и главная часть мышьякосодержащих руд перерабатывается в белый мышьяк, то есть в триоксид мышьяка — мышьяковистый ангидрид As2О3.
Применение
Мышьяк используется для легирования сплавов свинца, идущих на приготовление дроби, так как при отливке дроби башенным способом капли сплава мышьяка со свинцом приобретают строго сферическую форму, и кроме того, прочность и твёрдость свинца возрастают. Мышьяк особой чистоты (99,9999 %) используется для синтеза ряда ценных и важных полупроводниковых материалов — арсенидов и сложных алмазоподобных полупроводников. Сульфидные соединения мышьяка — аурипигмент и реальгар — используются в живописи в качестве красок и в кожевенной отрасли промышленности в качестве средств для удаления волос с кожи. В пиротехнике реальгар употребляется для получения «греческого», или «индийского», огня, возникающего при горении смеси реальгара с серой и селитрой (ярко-белое пламя). Многие из мышьяковых соединений в очень малых дозах применяются в качестве лекарств для борьбы с малокровием и рядом тяжелых заболеваний, так как оказывают клинически значимое стимулирующее влияние на ряд функций организма, в частности, на кроветворение. Из неорганических соединений мышьяка мышьяковистый ангидрид может применяться в медицине для приготовления пилюль и в зубоврачебной практике в виде пасты как некротизирующее лекарственное средство. Этот препарат называли «мышьяк» и применялся в стоматологии при удалении нерва. В настоящее время препараты мышьяка применяются в зубоврачебной практике редко из-за токсичности. Разработаны и применяются другие методы безболезненной денервации зуба под местной анестезией.
Мышьяк, свойства атома, химические и физические свойства
Мышьяк, свойства атома, химические и физические свойства.
74,92160(2) 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 3
Мышьяк — элемент периодической системы химических элементов Д. И. Менделеева с атомным номером 33. Расположен в 15-й группе (по старой классификации — главной подгруппе пятой группы), четвертом периоде периодической системы.
Атом и молекула мышьяка. Формула мышьяка. Строение атома мышьяка:
Мышьяк – неметалл. Относится к полуметаллам. Относится к группе пниктогенов.
Мышьяк обозначается символом As.
Как простое вещество мышьяк при нормальных условиях представляет собой хрупкий полуметалл стального цвета с зеленоватым оттенком, либо жёлтого или чёрного цвета.
Молекула мышьяка одноатомна.
Химическая формула мышьяка As.
Строение атома мышьяка. Атом мышьяка состоит из положительно заряженного ядра (+33), вокруг которого по четырем оболочкам движутся 33 электрона. При этом 28 электронов находятся на внутреннем уровне, а 5 электронов – на внешнем. Поскольку мышьяк расположен в четвертом периоде, оболочек всего четыре. Первая – внутренняя оболочка представлена s-орбиталью. Вторая – внутренняя оболочка представлена s- и р-орбиталями. Третья – внутренняя оболочка представлена s-, р- и d-орбиталями. Четвертая – внешняя оболочка представлена s- и р-орбиталями. На внешнем энергетическом уровне атома мышьяка на 4s-орбитали находятся два спаренных электрона, на 4p-орбитали – три неспаренных электрона. В свою очередь ядро атома мышьяка состоит из 33 протонов и 42 нейтрона. Мышьяк относится к элементам p-семейства.
Радиус атома мышьяка (вычисленный) составляет 114 пм.
Атомная масса атома мышьяка составляет 74,92160(2) а. е. м.
Мышьяк известен с глубокой древности. Арабскими алхимиками мышьяк использовался до 815 года н. э.
Мышьяк и многие его соединения ядовиты и канцерогенны.
Изотопы и модификации мышьяка:
Свойства мышьяка (таблица): температура, плотность, давление и пр.:
– α-мышьяк, серый мышьяк (наиболее распространенная, металлическая модификация) с ромбоэдрической (тригональной) кристаллической решёткой,
– β-мышьяк, чёрный мышьяк (неметаллическая модификация) в виде: стеклянной аморфной чёрной формы мышьяка или метастабильной орторомбической чёрной формы мышьяка,
4,9 г/см 3 (при 20 °C и иных стандартных условиях , состояние вещества – твердое тело) – чёрный мышьяк,
1,97 г/см 3 (при 20 °C и иных стандартных условиях , состояние вещества – твердое тело) – жёлтый мышьяк
0,344 Дж/г·K (при 0-100 °C)
50,2 Вт/(м·К) (при 300 K)
100* Данные в таблице приводятся применительно к серому мышьяку, если не указано иное.
205* Эмпирический радиус атома мышьяка согласно [1] и [3] составляет 119 пм и 139 пм соответственно.
206* Ковалентный радиус мышьяка согласно [1] и [3] составляет 119±4 пм и 120 пм соответственно.
401* Плотность серого мышьяка согласно [3] составляет 5,73 г/см 3 (при 0 °C и иных стандартных условиях , состояние вещества – твердое тело).
404* Температура сублимации мышьяка согласно [3] и [4] составляет 612,85 °С (886 K, 1135,13 °F) и 615 °C (888,15 К, 1139 °F) соответственно.
407* Удельная теплота плавления (энтальпия плавления ΔHпл) мышьяка согласно [4] составляет 22 кДж/моль.
408* Удельная теплота испарения (энтальпия кипения ΔHкип) мышьяка согласно [3] и [4] составляет 32,4 кДж/моль и 32 кДж/моль соответственно.
410* Молярная теплоёмкость мышьяка согласно [3] составляет 25,05 Дж/(K·моль).



















