Миостатин как понизить в организме
Чтобы восстановить состарившиеся мышцы, заблокируйте миостатин
Найден ключ к восполнению возрастной потери мышечной массы
Результаты нового исследования, проведенного учеными Университета Джонса Хопкинса (Johns Hopkins University), убедительно подтверждают теорию о том, что возрастную потерю мышечной массы можно восполнить в условиях отсутствия полностью функционального ресурса мышечных стволовых клеток.
У взрослых млекопитающих, включая человека, мышечные стволовые клетки, известные как сателлитные клетки, как правило, находятся в спящем состоянии. Физические упражнения или травма стимулируют их деление и слияние либо друг с другом, либо с близлежащими мышечными волокнами, что позволяет увеличить или заместить потерянную мышечную массу. При атрофических мышечных расстройствах, таких как мышечная дистрофия, дегенерация мышц сначала активирует регенерацию потерянных тканей клетками-сателлитами, но в конечном итоге этот регенеративный ресурс исчерпывается и баланс смещается в сторону дегенерации.
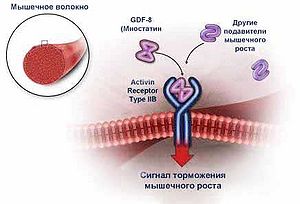
Механизм сохранения и увеличения мышечной массы в нормальных условиях, при отсутствии травм, включая роль миостатина – секретируемого мышечными клетками белка, останавливающего рост мышц, – остается малоизученным. Блокирование функции миостатина у нормальных мышей приводит к увеличению массы мышц на 25-50 процентов. Но какие именно клетки получают сигнал миостатина и реагируют на него, остается неизвестным. Сегодня в этом подозреваются как сателлитные, так и сами мышечные клетки.
Чтобы выяснить, необходимы ли для реализации функции миостатина сателлитные клетки, американские ученые использовали три подхода. Во-первых, они исследовали специально выведенных мышей с тяжелыми дефектами либо в функции, либо количестве сателлитных клеток. При блокировании функции миостатина (с помощью химических веществ или генной инженерии) у обоих типов мышей мышечная масса по-прежнему значительно увеличивалась по сравнению с таковой у мышей с нормальной функцией сателлитных клеток. Эти результаты означали, что миостатин может действовать, по крайней мере, частично, независимо от сателлитных клеток.

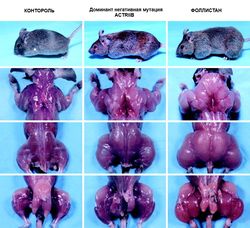
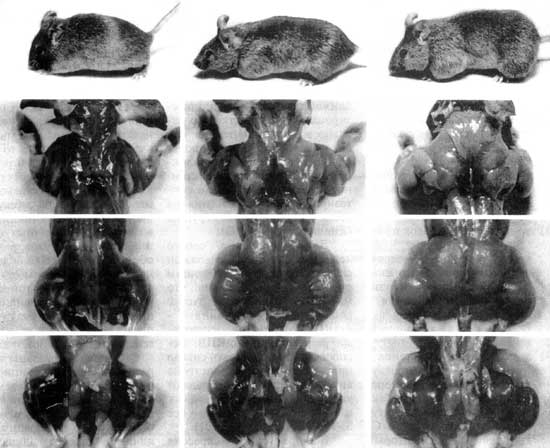
Фото: Se-Jin Lee Lab.
Во-вторых, ученые предположили, что, если миостатин непосредственно подавляет рост сателлитных клеток, их число в отсутствие миостатина должно увеличиться. Исследователи пометили сателлитные клетки стойким красителем, а затем подавили функцию миостатина химическим веществом. Как и ожидалось, мышечная масса мышей значительно увеличилась, но количество сателлитных клеток осталось прежним. Не наблюдалось и их более активного слияния с мышечными волокнами. По словам профессора Ли, эти результаты убедительно доказывают, что миостатин не подавляет пролиферацию сателлитных клеток.
В-третьих, для дальнейшего подтверждения своей теории о том, что миостатин действует, прежде всего, через мышечные клетки, а не через клетки-сателлиты, ученые вывели мышей с мышечными клетками, лишенными рецепторов миостатина. Если большинство рецепторов миостатина находится на сателлитных клетках, удаление рецепторов с мышечных клеток не должно было бы изменить активность миостатина. Но исследователи наблюдали умеренное, но статистически значимое увеличение мышечной массы, что еще раз доказывало, что важными приемниками сигналов миостатина являются сами мышечные клетки.
Профессор Ли отмечает, что, поскольку полученные им результаты не дают никаких доказательств, что клетки-сателлиты имеют первостепенное значение для молекулярного пути миостатина, даже пациенты с пониженной мышечной массой, обусловленной подавлением функции сателлитных клеток, способны к некоторому восстановлению мышечного тонуса с помощью лекарственной терапии, блокирующей активность миостатина.
Все мы, по мере старения, теряет мышечную массу, и самым распространенным объяснением этому является потеря сателлитных клеток.
«Можно ли увеличить мышечную массу, подвижность и независимость нашего стареющего населения, заблокировав путь миостатина?», – задается вопросом профессор Ли. – Наши эксперименты на мышах показывают, что эта стратегия действительно может решить проблемы, связанные с потерей сателлитных клеток».
Миостатин
Содержание
Миостатин (GDF-8) [ править | править код ]
Исследования на животных показывают, что блокирование действия миостатина приводит к значительному увеличению сухой мышечной массы с практически полным отсутствием жировой прослойки. [3]
Борзая с мутацией гена миостатина
Знаменитый бодибилдер Flex Wheeler с врожденной мутацией гена миостатина
Мальчик 12 лет, как утверждалось с мутацией гена миостатина
Слева Ричард Сандрак в 12 лет, справа в 24 года: мышцы исчезли, когда он перестал тренироваться
Блокаторы миостатина [ править | править код ]
В настоящее время ведется разработка целого ряда блокаторов действия миостатина, 
Блокатор миостатина MYO-029 (Stamulumab) [ править | править код ]
В начале 2005 года Wyeth Pharmaceuticals при дополнительном финансировании MDA начала фазу 1-2 клинических исследований безопасности и переносимости MYO-029 (Stamulumab) на 116 испытуемых. Данные клинических испытаний были опубликованы только в январе 2008 года.
Препарат показал себя безопасным и хорошо переносимым в трех различных дозировках, о чем сообщено в отчете, опубликованном Kathryn Wagner с коллегами из Johns Hopkins University School of Medicine в Baltimore в журнале Annals of Neurology [4]
Однако в марте 2008 года, после окончания клинических испытаний компания объявила о приостановке развития проекта MYO-029 (Stamulumab), так как ни у кого из участвующих в исследовании не было статистически значимого улучшения силы или роста мышц.
Элементы рецепторов ACVR2B как блокаторы миостатина [ править | править код ]
Большой потенциал имеет новый препарат ACVR2B, который представляет собой раствор элементов рецепторов к миостатину. Молекулярные элементы ACVR2B имеют участок, схожий с активным центром рецептора и связываются со свободным миостатином, блокируя его способность активировать рецепторы. Данный препарат был создан в 2005 году, под руководством все того же доктора Se-Jin Lee, Johns Hopkins University School of Medicine в Baltimore. Se-Jin Lee надеется, что ACVR2B может использоваться в ближайшем будущем и на людях, тогда как по состоянию на 2005 год он уже доказал высокую эффективность на лабораторных мышах. Команда доктора Se-Jin Lee апробировала различные дозы ACVR2B на 49 мышах и зафиксировала мышечный прирост после четырех недель применения препарата. Максимальные показатели мышечного прироста были достигнуты при двух инъекциях в неделю, в дозировке 50 мкг на килограмм массы тела. Мышечная масса этих мышей увеличилась на 61% по сравнению с исходной. [5]
ACE-031 [ править | править код ]
ACE-031 еще один перспективный препарат класса блокаторов миостатина, он представляет собой раствор экстрацеллюлярных частей рецепторов ActRIIB соединенных с Fc фрагментом иммуноглобулина G. Путем блокирования сигнала через рецептор ActRIIB, препарат увеличивает мышечную массу и силу. Предварительные испытания ACE-031 продемонстрировали высокую эффективность на экспериментальных моделях с животными.
Клинические испытания ACE-031 для лечения миодистрофии были прекращены в мае 2013 года в связи с развитием побочных эффектов (дилатация сосудов кожи, кровотечения из носа и десен). [6] В продаже доступны кустарные препараты от китайского производителя.
Модифицированные пропептиды миостатина [ править | править код ]
Пробы проводились только на животных, и данных о применении препаратов данной группы на людях пока нет.
Выводы для спортсменов [ править | править код ]

1. Недостаточная доказательная база. Многие исследования дают диаметрально противоположные выводы, поэтому пока достоверных данных в этой области очень мало.
2. Побочные эффекты. Сейчас еще рано судить о безопасности выключения действия миостатина. Возможно, это может приводить к отсроченным осложнениям различного рода, к примеру, гипертрофия миокарда. Так же последние работы показали, что интенсивный мышечный рост приводит к увеличению частоты травм связочного аппарата, который остается на таком же уровне развития и рассчитан на относительно меньшие нагрузки.
3. Низкая селективность. Как уже было замечено, миостатин является частью очень обширной метаболической системы, где многие элементы имеют схожее строение и дублируют функцию других. Применяя препараты, ингибирующие действие миостатина, можно получить сбой в работе других элементов метаболической системы. Иными словами, учитывая довольно широкий диапазон компетенции данной метаболической системы, помимо мышечного роста существует вероятность многочисленных серьезных побочных эффектов со стороны всех систем органов и тканей.
Блокаторы миостатина в спортивном питании [ править | править код ]
В то время, как в научном мире идут ярые споры и активно ведутся испытательные работы, мир спортивной индустрии активно производит абсолютно безопасные и «эффективные» блокаторы миостатина.
Myo-Blast, по заявлению производителя, содержит самую высокую дозу наиболее мощного средства миостатин-нейтрализующего средства, известного как — Myozap CSP3.
Выдержка из описания:

2. Все современные антагонисты миостатина белковой природы, поэтому они не принимаются внутрь, так как в этом случае активное вещество было бы неминуемо разрушено пищеварительными ферментами.
 Эффективные блокаторы миостатина [ править | править код ]
Эффективные блокаторы миостатина [ править | править код ]
В 2009 году было опубликовано исследование, проведенное иранскими учеными. Они выявили, что миостатин в значительной степени подавляется при дополнительном приеме креатина. [7]
Hulmi JJ и Tannerstedt J доказали, что протеин блокирует синтез миостатина при систематическом употреблении тренирующимися людьми. [8]

Читайте также [ править | править код ]
Предупреждение [ править код ]

Читательской аудитории этого журнала хорошо известно значение поддержания нормального функционального состояния скелетной мускулатуры для здоровья и долголетия. Известны им и различные состояния, сопровождающиеся потерей или риском потери мышечной массы, такие, как:
Очевидно, что знание способов регуляции величины мышечной массы имело бы огромное терапевтическое значение и означало бы значительное снижение риска осложнении и даже летальных исходов.
Рис. 1. Бык породы Belgian Blue (Бельгийская голубая).
Так, например, установлено, что у пациентов с хроническими обструктивными легочными заболеваниями именно уменьшение индекса мышечной массы ниже определенной величины, а не индекса массы тела в целом, наиболее точно коррелирует со смертностью (Marquis К., et al., 2002).
Наряду со значительным увеличением всех мышечных групп видно практически полное отсутствие подкожной жировой ткани.
После этого открытия в том же 1997 году в нескольких лабораториях клонировали и установили последовательность гена миостатина у крупного рогатого скота пород «Бельгийская голубая» и Piedmontese. Было обнаружено, что у этих животных имеются мутации в гене миостатина (различные в каждой из пород), которые тем или иным образом приводят к отсутствию функционально активного миостатина (McPherron A., Lee S-J., 1997; Grobet L. et al., 1997; Kambadur R. et al., 1997). В отличие от мышей с поврежденным геном миостатина у этих пород происходит только гиперплазия мышечной ткани без гипертрофии. Хотя применительно к этому мясному скоту используют термин «фенотип удвоенной мышечной массы», суммарное увеличение всех мышц составляет не более 40% по сравнению с другими мясными породами, но и это, безусловно, неоценимо для мясного животноводства. Рис. 1 показывает, как отсутствие функционально активного миостатина (ген миостатина работает, но синтезированный белок неактивен) приводит к увеличению мышечной массы.
Было установлено, что миостатин по своей структуре относится к белкам типа TGF-β (Transforming Growth Factor-beta, трансформирующий фактор роста-бета), которые представляют собой секретируемые факторы, необходимые как в ходе эмбриогенеза, так и во взрослом состоянии для тканевого гомеостаза.
Миостатин имеет общие структурные свойства с другими белками семейства TGF-β:
Процесс экспрессии миостатина, возможно, регулируется белком Titin-cap (Nicholas G. et al., 2002), так как установлено, что синтез этого белка уменьшает выход миостатина из клеток. Секретированный в виде комплекса с пропептидом миостатин неактивен, так как не может связываться со своим рецептором. Для проявления активности миостатин должен быть отделен от пропептида. Активация миостатина осуществляется в результате расщепления пропептида протеазами типа катепсина D.
Считается, что основная масса синтезированного миостатина проявляет свое действие аутокринным и паракринным образом, т.е. миостатин действует внутри и в районе ближайшего окружения синтезировавшей его клетки, но недавно в экспериментах in vivo доказана возможность проявления его активности эндокринным образом, т.е. системное воздействие локально синтезированного миостатина на все мышечные группы (Zimmers Т. et al, 2002).
Для проявления своего действия миостатин должен связаться с соответствующим ему рецептором. Показано, что миостатин взаимодействует с рецепторами активина ActRIIB. Мыши с измененными рецепторами ActRIIB, неспособными передавать сигнал при связывании миостатина внутрь клетки, также обладают увеличенной мускулатурой, как и миостатин-ноль мыши (Lee S.-J. & McPherron A., 2001).
В эмбриогенезе экспрессия гена миостатина начинается в прогениторных клетках мио-генной линии и продолжается во взрослых аксиальных и параксиальных мышцах (McPherron A. et al., 1997). При этом уровень синтеза миостатина различен в разных скелетных мышцах (Kambadur R. et al., 1997).
Последующие исследования обнаружили экспрессию гена миостатина в ряде других тканей. Показано, что миостатин присутствует в кардиомио-цитах и волокнах Пуркинье в сердце (Sharma M., et al., 1999), синтез мРНК миостатина обнаружен в молочных железах (Ji S, et al., 1998) и в адипоцитах (Kim HS, etal, 2001).
Можно предполагать, что половые различия в количестве секретируемого миостатина, наряду с другими факторами, влияют на половой диморфизм в развитии скелетной мускулатуры. При одинаковом уровне
Синтеза мРНК миостатина, т.е. уровне экспрессии гена миостатина, уровень секретированного миостатина выше у женщин, чем у мужчин (McMahon et al., 2002).
Поскольку экспрессия гена миостатина начавшаяся в эмбриогенезе продолжается в постнатальных мышцах и мышцах взрослого организма, то миостатин, по-видимому, играет существенную роль на всех стадиях миогенеза и в тканевом гомеостазе скелетной мускулатуры во взрослом состоянии при воздействии различных функциональных стимулов, включая обездвиживание. Для более ясного представления места миостатина в мышечном гомеостазе на рис. 3 и 4 приведена общая информация схематически представляющая миогенез и регенерацию мышечной ткани.
Рис. 3. Схематическое представление этапов развития и дифференцировки мышечной ткани.
На рис. 3 показаны этапы развития и дифференцировки мышечной ткани. Эта схема составлена для отображения процессов происходящих в эмбриогенезе, но с небольшими отличиями она справедлива и для мышц взрослого организма.
В мышечных волокнах количество цитоплазмы, приходящееся на одно ядро, находится в определенных достаточно узких пределах (мионуклеарный домен). Увеличение размеров волокна (гипертрофия) достигается благодаря слиянию пролиферирующих сателлитных клеток с волокном, так что размеры мионуклеарного домена остаются в тех же пределах, что и до гипертрофии. Стимулом для деления (пролиферации) сателлитных клеток у взрослых организмов является, в первую очередь, миотравма, в том числе на уровне отдельного мышечного волокна. Участие сателлитных клеток в ответе на миотравму представлено на рис. 4. Выходя из состояния покоя, сателлитные клетки начинают экспрессировать миоген-ные маркеры, т.е., активируются гены характерные для миобластов. В процессе регенерации поврежденных скелетных мышц сателлитные клетки сливаются с существующими мышечными волокнами (гипертрофия) или между собой, создавая новые волокна (гиперплазия).
Определяя долю сателлитных клеток в мышечной ткани удобнее сопоставлять миофиб-риллы и сателлитные клетки по числу ядер, поскольку мышечные волокна многоядерны. Во взрослом состоянии ядра сателлитных клеток составляют 2-7% от общего числа ядер в различных мышцах. При рождении р ядра сателлитных клеток составляют около 30% от общего числа ядер в мышцах нижних конечностей (Schultz E. & McCormick K.M., 1994). Эти неонатальные сателлитные клетки пролиферируют и сливаются с растущими мышечными волокнами, привнося в них дополнительные ядра в ходе постнатального роста скелетных мышц.
Рис.4. Схематическое представление участия сателлитных клеток в регенерации мышечных волокон.
В ответ на миотравму сателлитные клетки активируются и пролиферируют. Часть клеток после деления возвращается в состояние покоя (для восстановления пула сателлитных клеток). Основная часть клеток в результате хемотаксиса мигрирует к поврежденным участкам и, в зависимости от степени повреждения, или сливается с поврежденным мышечным волокном или сателлитные клетки сливаются друг с другом, образуя новые волокна. Ядра недавно слившихся сателлитных клеток находятся в центре волокон, затем, по мере восстановления внутриклеточных структур волокна, мигрируют к периферии.
Таким образом, сателлитные клетки обеспечивают поддержание функционального состояния скелетных мышц взрослого организма, необходимы для восстановления поврежденных мышечных волокон и являются источником дополнительных ядер при гипертрофии мышц в результате тренировок. Гипертрофия и/или гиперплазия скелетных мышц у животных с отсутствием функционально активного миостатина доказывает, что миостатин влияет на пролиферацию сателлитных клеток, поскольку постнатальный рост мышц и увеличение числа ядер в мышечных волокнах в процессе развития до взрослого состояния происходит благодаря пролиферации сателлитных клеток.
При активации сателлитных клеток (выходе из состояния покоя) в них начинают работать гены характерные для миобластов и, таким образом, сателлитные клетки становятся, по сути, миобластами. Это означает, что степень пролиферации сателлитных клеток во взрослых мышцах также ограничивается миостатином, как и пролиферация миобластов в эмбриогенезе. Показано, что и белок TGF-β ингибирует пролиферацию сателлитных клеток в культуре (Allen R.E. & Boxhorn L.K., 1987).
Роль миостатина в гомеостазе зрелых мышечных волокон в полной мере пока не выяснена, но имеется ряд работ по исследованию уровня синтеза как мРНК миостатина, так и самого миостатина в мышцах во взрослом состоянии на животных моделях и у человека при различных физиологических состояниях.
Так системная сверхэкспрессия миостатина у мышей в течение двух недель приводит к потере свыше 30% общей массы тела и 50% по мышечной массе, то есть картина практически идентичная синдрому кахексии у человека. Эта работа доказала, что миостатин может действовать эндокринным образом. Введение ингибиторов миостатина пропептида или фоллистатина значительно замедляет потерю мышечной массы при повышенном уровне миостатина. Также важно отметить, что наряду с потерей мышечной массы происходит практически полная потеря подкожного жира, что также согласуется с данными о влиянии миостатина на дифференцировку адипоцитов (Zimmers Т.А. et al., 2002).
У людей разных возрастных категорий уровень миостатина в сыворотке крови наиболее высок у мужчин и женщин старше 72 лет и коррелирует со степенью саркопении. У мужчин и женщин среднего возраста уровень миостатина в сыворотке в свою очередь выше по сравнению с молодыми людьми. Индексы нежировой массы тела и мышечной массы тела обратно пропорционально коррелируют с сывороточным миостатином во всех возрастных категориях. Эти данные позволяют рассматривать миостатин не просто как биомаркер возрастной саркопении, но как супрессор мышечной массы. (Yarasheski K.E., et al., 2002).
Внутримышечная и сывороточная концентрации миостатина увеличены у больных СПИДом в стадии, когда наблюдается потеря мышечной массы, при этом концентрация миостатина обратно пропорционально коррелирует с индексом нежировой массы тела. Эти результаты показывают, что миостатин вносит вклад в потерю мышечной массы при СПИДе. (Gonzalez-CadavidN.E.et al., 1998).
В прямых экспериментах на крысах выявлено, что потеря мышечной массы, происходящая при космическом полете, связана с увеличением уровня миостатина в скелетных мышцах (2-5 кратное в различных мышцах к 17-му дню полета). Эти результаты показывают, что миостатин один из основных элементов в многофакторной патофизиологии мышечной атрофии происходящей при космическом полете (Lalani R., et al., 2000).
В наземных экспериментах на людях установлено, что к 25-му дню неподвижного режима (в качестве модели космического полета) уровень миостатина повышается на 12% (ZachwiejaJ. J. etal., 1999).
Другое заключение состоит в том, что синтез миостатина коррелирует с типом волокон, т.е. синтез миостатина при иммобилизации мышц у мышей коррелирует с изоформой тяжелой цепи миозина IIb.
На мышиной модели мышечной дистрофии Дюшена (мыши линии mdx) показано, что блокада эндогенного миостатина путем внутрибрюшинных инъекций антител к миостатину в течение трех месяцев приводит к увеличению мышечной массы, размеров и силы мышц (Bogdanovich S., et al., 2002). Гибриды mdx-мышей с миостатин-ноль мышами имеют значительно лучшее состояние мускулатуры, чем исходные mdx-мыши (Wagner K.R. et al., 2002). Нормализация состояния мышц у mdx-мышей путем блокады миостатина или скрещивания с миостатин-ноль мышами открывает новые возможности для лечения патологий сопровождающихся потерей мышечной массы.
Очевидно, что искусственное ингибирование активности миостатина повлечет за собой революционные изменения в медицине и спорте и, возможно, будет использоваться в широких терапевтических целях (Lee S. J., McPherron А.С., 2001).
По материалам журнала «Физкультура в профилактике, лечении и реабилитации» №1 И. М.Ундрицов, В. М. Ундрицов, Э. Ф. Андреев. Московский центр медицинской косметологии и хирургии ЗАО «Лантан-Мед». НП Институт эффективного долголетия, Москва, Россия.