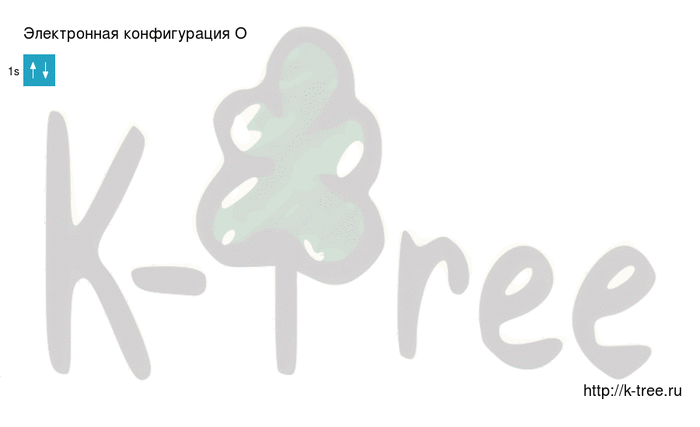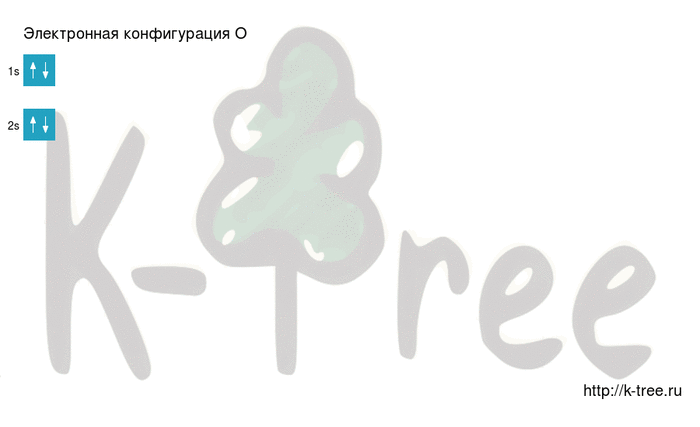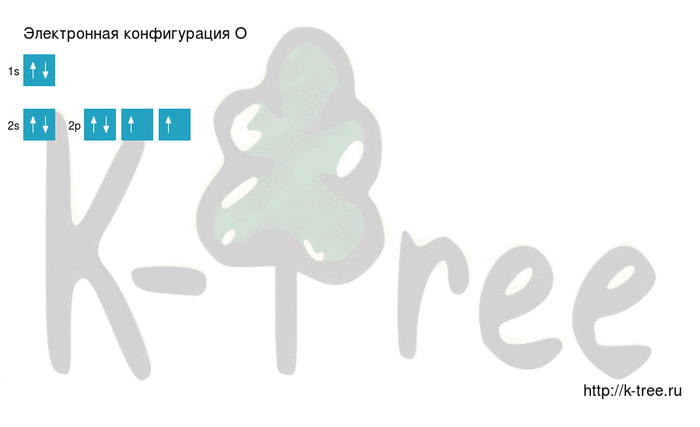кислород номер в таблице
Кислород
Газ без цвета, без запаха, составляет 21% воздуха.
Общая характеристика элементов VIa группы
От O к Po (сверху вниз в периодической таблице) происходит увеличение: атомного радиуса, металлических, основных, восстановительных свойств. Уменьшается электроотрицательность, энергия ионизации, сродство к электрону.
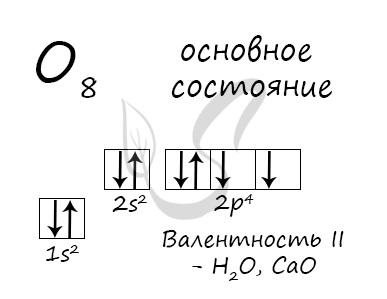
Основное состояние атома кислорода
У атома кислорода (как и атомы азота, фтора, неона) нет возбужденного состояния, так как отсутствует свободная орбиталь с более высоким энергетическим уровнем, куда могли бы перемещаться валентные электроны.
Атом кислорода имеется два неспаренных электрона, максимальная валентность II.
Природные соединения
Получение
В промышленности кислород получают из сжиженного воздуха. Также активно применяются кислородные установки, мембрана которых устроена как фильтр, отсеивающие кислород (мембранная технология).
В лаборатории кислород получают разложением перманганата калия (марганцовки) или бертолетовой соли при нагревании. Применяется реакция каталитического разложения пероксида водорода.
На подводных лодках для получения кислорода применяют следующую реакцию:
Химические свойства
Является самым активным неметаллом после фтора, образует бинарные соединения со всеми элементами кроме гелия, неона, аргона. Чаще всего реакции с кислородом экзотермичны (горение), ускоряются при повышении температуры.
Во всех реакциях, кроме взаимодействия со фтором, кислород проявляет себя в качестве окислителя.
F + O2 → OF2 (фторид кислорода, O +2 )
В реакциях кислорода с металлами образуются оксиды, пероксиды и супероксиды. Реакции с активными металлами идут без нагревания.
Известна реакция горения воды во фторе.
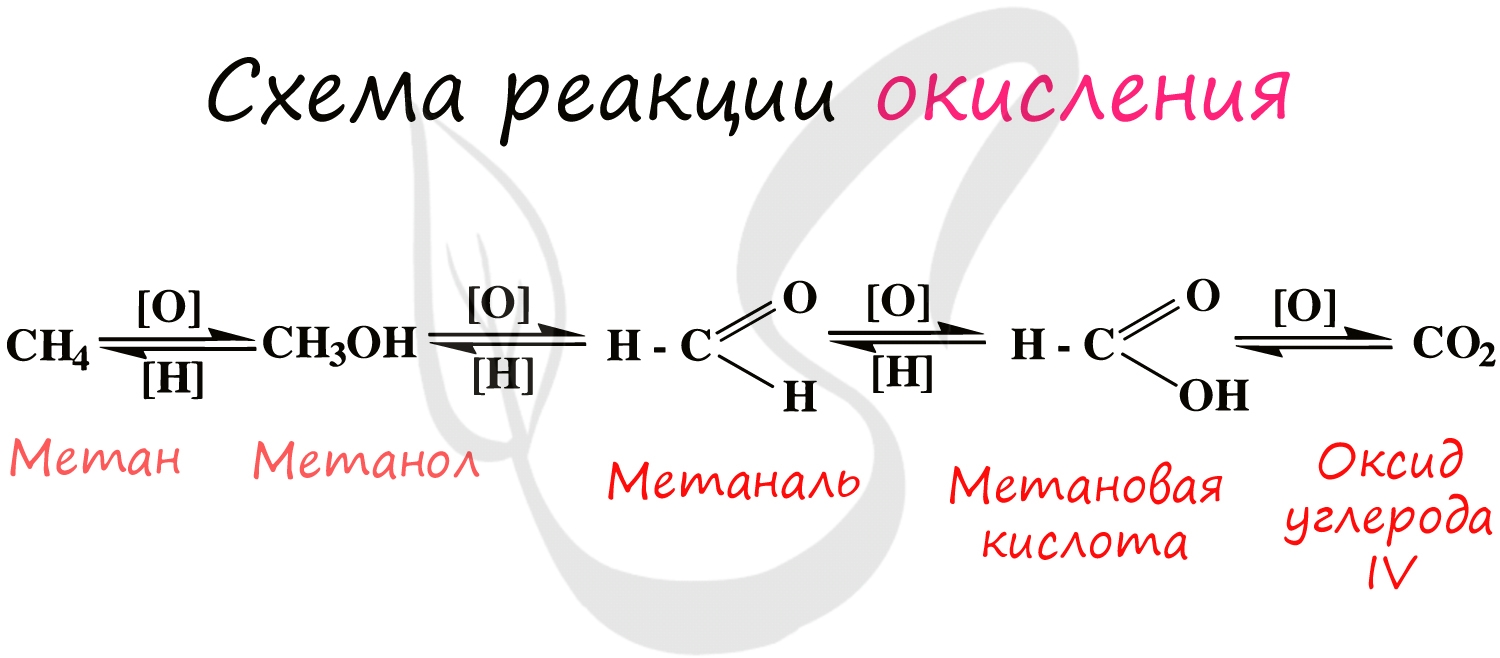
Все органические вещества сгорают с образованием углекислого газа и воды.
Процесс можно остановить на любой стадии в зависимости от желаемого результата.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Кислород O
Кислород в таблице менделеева занимает 8 место, в 2 периоде.
| Символ | O |
| Номер | 8 |
| Атомный вес | 15.9990300 |
| Латинское название | Oxygenium |
| Русское название | Кислород |
Как самостоятельно построить электронную конфигурацию? Ответ здесь
Электронная схема кислорода
Порядок заполнения оболочек атома кислорода (O) электронами: 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d → 5p → 6s → 4f → 5d → 6p → 7s → 5f → 6d → 7p.
Кислород имеет 8 электронов, заполним электронные оболочки в описанном выше порядке:
2 электрона на 1s-подуровне
2 электрона на 2s-подуровне
4 электрона на 2p-подуровне
Степень окисления кислорода
Ионы кислорода
Валентность O
Атомы кислорода в соединениях проявляют валентность II, I.
Валентность кислорода характеризует способность атома O к образованию хмических связей. Валентность следует из строения электронной оболочки атома, электроны, участвующие в образовании химических соединений называются валентными электронами. Более обширное определение валентности это:
Число химических связей, которыми данный атом соединён с другими атомами
Валентность не имеет знака.
Квантовые числа O
Квантовые числа определяются последним электроном в конфигурации, для атома O эти числа имеют значение N = 2, L = 1, Ml = 2, Ms = ½
Видео заполнения электронной конфигурации (gif):
Результат:
Энергия ионизации
Перейти к другим элементам таблицы менделеева
Кислород как химический элемент
Кислород – химический элемент, свойства которого будут рассмотрены в следующих нескольких параграфах. Обратимся к Периодической Системе химических элементов Д.И. Менделеева. Элемент кислород расположен во 2 периоде, VI группе, главной подгруппе.
Там же указано, что относительная атомная масса кислорода равна 16. По порядковому номеру кислорода в Периодической Системе можно легко определить количество электронов, содержащихся в его атоме, заряд ядра атома кислорода, количество протонов. Валентность кислорода в большинстве соединений равна II. Атом кислорода может присоединять два электрона и превращаться в ион:
Стоит отметить, что кислород – самый распространенный элемент на нашей планете. Кислород входит в состав воды. Морские и пресные воды на 89% по массе состоят из кислорода. Кислород входит в состав множества минералов и горных пород. Массовая доля кислорода в земной коре составляет около 47%. В воздухе кислорода содержится около 23% по массе.
Физические свойства кислорода
При взаимодействии двух атомов кислорода образуется устойчивая молекула простого вещества кислорода O2. Данное простое вещество, как и элемент, называется кислородом. Не путайте кислород-элемент, и кислород – простое вещество!
По физическим свойствам кислород – бесцветный газ без запаха и вкуса. Практически нерастворим в воде (при комнатной температуре и нормальном атмосферном давлении растворимость кислорода составляет около 8 мг на один литр воды). Кислород растворим в воде – в 1 л воды при температуре 20°С растворяется 31 мл кислорода (0,004% по массе). Однако этого количества достаточно для дыхания рыб, живущих в водоемах. Газообразный кислород немного тяжелее воздуха:
1 л воздуха при температуре 0°С и обычном давлении весит 1,29 г, а 1 л кислорода – 1,43 г.
Кислород проявляет интересные свойства при сильном охлаждении. Так, при температуре –183°С кислород конденсируется в прозрачную подвижную жидкость бледно- голубого цвета. Если жидкий кислород охладить еще сильнее, то при температуре –218°С кислород «замерзает» в виде синих кристаллов. Если температуру постепенно повышать, то при –218°С, твердый кислород начнет плавится, а при –183°С – закипит. Следовательно, температуры кипения и конденсации, а также температуры замерзания и плавления для веществ являются одинаковыми.
Для хранения и транспортировки жидкого кислорода используют так называемые сосуды Дьюара. Сосуды Дьюара используют для хранения и транспортировки жидкостей, температура которых должна длительное время оставаться постоянной. Сосуд Дьюара носит имя его изобретателя, шотландского физика и химика Джеймса Дьюара. Простейшим сосудом Дьюара является бытовой термос. Устройство сосуда довольно простое: это колба, помещенная в большую колбу. Из герметичного пространства между колбами откачивается воздух. Благодаря отсутствию воздуха между стенками колб, жидкость, налитая во внутреннюю колбу, долгое время не остывает или не нагревается.
Кислород — парамагнитное вещество, то есть в жидком и твердом состояниях он притягивается магнитом
В природе существует еще одно простое вещество, состоящее из атомов кислорода. Это озон. Химическая формула озона О3.
Озон, так же как и кислород, в обычных условиях – газ. Озон образуется в атмосфере во время грозовых разрядов. Характерный запах свежести после грозы является запахом озона. Если озон получить в лаборатории и собрать значительное количество его, то в больших концентрациях озон будет иметь резкий неприятный запах. Получают озон в лаборатории в специальных приборах – озонаторах.
Озонатор – это стеклянная трубка, в которую подают ток кислорода, и создают электрический разряд. Электрический разряд превращает кислород в озон: В отличие от бесцветного кислорода, озон – газ голубого цвета. Растворимость озона в воде составляет около 0,5 л газа на 1 литр воды, что значительно больше, чем у кислорода. С учетом этого свойства озон применяется для обеззараживания питьевой воды, так как оказывает губительное действие на болезнетворные микроорганизмы.
При низких температурах, озон ведет себя аналогично кислороду. При температуре –112°С он конденсируется в жидкость фиолетового цвета, а при температуре –197°С кристаллизуется в виде темно-фиолетовых, почти черных кристаллов Таким образом, можно сделать вывод, что атомы одного и того же химического элемента могут образовывать разные простые вещества.
Аллотропия — это явление существования химического элемента в виде нескольких простых веществ
Простые вещества, образованные одним и тем же элементом, называют аллотропными модификациями
Значит, кислород и озон – аллотропные модификации химического элемента кислорода. Существуют данные, что при сверхнизких температурах, в жидком или твердом состоянии кислород может существовать в виде молекул О4 и О8.
Круговорот кислорода в природе
Количество кислорода в атмосфере постоянно. Следовательно, расходующийся кислород постоянно пополняется новым. Важнейшими источниками кислорода в природе является углекислый газ и вода. Кислород попадает в атмосферу главным образом в результате процесса фотосинтеза, протекающего в растениях, согласно схеме реакции:
Кислород может образовываться и в верхних слоях атмосферы Земли: вследствие воздействия солнечного излучения, водяные пары частично разлагаются с образованием кислорода. Кислород расходуется при дыхании, сжигании топлива, окислении различных веществ в живых организмах, окислении неорганических веществ, содержащихся в природе. Большое количество кислорода расходуется в технологических процессах, таких как, например, выплавка стали.
Итог статьи:
Кислород как химический элемент таблицы Менделеева
Как был открыт кислород
Истоиия открытия такого химического элемента как кислород довольно запутанная. Первые эксперименты о взаимосвязи горения и кислорода были описаны еще во II веке до нашей эры. Греческий писатель, называемый Филоном из Византии, в своей работе заметил, что переворачивание сосуда над горящей свечой и окружение шеи сосуда водой приводит к тому, что в шею поднимается немного воды. Спустя много веков Леонардо Да Винчи повторяя опыты Филона заметил, что при горении и дыхании расходуется значительная часть воздуха и пламя через какое-то время гаснет.
В конце XVII века Роберт Бойл доказал, что воздух необходим для горения. В период с 1641 по 1679 год английский химик Джон Мейоу усовершенствовал работу Бойла. Он доказал, что для горения нужна только часть воздуха, которую он назвал spiritus nitroaereus. В одном эксперименте он обнаружил, что размещение мыши или зажженной свечи в закрытом контейнере над водой вызывает подъем воды и заменяет одну четырнадцатую объема воздуха перед тем, как погасить огонь. Исходя из этого он предположил, что nitroaereus необходимо как для горения, так и для дыхания.
Официальное открытие
Такие великие ученые как Михаил Ломоносов, Роберт Гук, Пьер Байен в своих экспериментах в XVII – XVIII веках получали кислород во время опытов, но никто из них не обозначил его как отдельный элемент.
Михаил Сендивогиус
Возможным первооткрывателем кислорода можно считать польского алхимика, философа и врача Михаила Сендивогиуса. В своей работе 1604 года под названием «De Lapide Philosophorum Tractatus duodecim e naturae fonte et manuali experiencetia depromti» он описал вещество содержащееся в воздухе. Сендивогиус открыл его в ходе опытов окисления нитрата калия, как газообразный продукт разложения. Новое вещество он назвал «cibus vitae», что в переводе означает пища жизни. Признания это эткрытие так и не получило.
Карл Вильгельм Шееле
На сегодняшний день, открытие кислорода присуждено шведскому фармацевту Карлу Вильгельму Шееле. В период с 1771 по 1772 год Карл получал кислород путем нагревания оксида ртути и оксидов нитратов. Шееле называл полученный в ходе опытов газ «Огненным воздухом». Такое название кислород получил потому, что на тот момент он был единственным известным реагентом поддерживающим горение. В 1777 году было опубликовано издание с опытами Шееле с названием «Трактат о воздухе и огне».
Джозеф Пристли
Еще одним возможным первооткрывателем можно считать Джозефа Пристли. 1 августа 1774 года британский священнослужитель сфокусировал солнечный свет на все том же оксиде ртути в стекляной трубке. При достаточном нагревании высвобождался газ, который Пристли назвал «дефлогистизированный воздух». Он отметил, что в этом газе свечи горели ярче и пламя было более активно. Британский священнослужитель даже вдохнул этот газ и отметил что он почти ничем не отличается от воздуха. Единственным отличием он установил, что дышалось ему гораздо легче чем обычным воздухом. Свои наработки он опубликовал в 1775 году под названием «Отчет о дальнейших открытиях в воздухе». Некоторая часть ученого мира утверждает именно Пристли первооткрывателем кислорода.
Антуан Лавуазье
Еще одним представителем первооткрывателей кислорода является французский химик Антуан Лавуазье. Он утверждал, что он так же, независимо от других ученых открыл новый элемент. Интересным является тот момент, что Шееле отправил письмо Лавуазье в котором описал свой опыт. Последний получение письма так и не подтвердил. В тоже время, только в октябре, Джозеф Пристли встречался с Лавуазье лично. При встрече Пристли поведал Лавуазье о своих опытах и новом газе который выделился при опыте. На самом деле, вклад Лавуазье в открытие достаточно велик. Он лично провел качественные опыты и подтвердил наличие отдельного химического элемента. Именно он дал название этому элементу Oxygen, который используется и по сей день. В переводе с греческого означает «жизненный воздух». Кто из этих ученых является первооткрывателем кислорода непонятно, но подытожил работу именно Антуан Лавуазье.
Где и как добывают кислород
Ежегодная масса потребления промышленного кислорода составляет около ста миллионов тонн. Способов получения кислорода очень много. В промышленных масштабах кислород O2 получают из воздуха двумя основными способами.
Первый способ заключается во фракционной перегонке сжиженного воздуха вместе с азотом N2 в виде пара, в то время как кислород остается в виде жидкости.
Вторым способом является прогонка чистого сухого воздуха через пару цеолитовых молекулярных сит. Это сито очищает воздух от примесей азота и оставляет газ в котором от 90 до 93% составляет O2. Одновременно с этим газообразный азот высвобождается из другого насыщенного азотом слоя цеолита путем снижения рабочего давления в камере и отвода через него части кислородного газа из слоя продувочного материала в обратном направлении потока. Такая процедура называется адсорбция при перепаде давления.
Распространенность кислорода
Говорить о распространенности кислорода можно очень много. Для начала этот химический элемент является третьим по распространенности во Вселенной. Его опережает только водород и гелий. Так же процент содержания кислорода в атмосфере Зеили составляет около 21%. Что же касается земной коры, то можно смело утверждать что половина от всех элементов земной коры является кислород. Только в земной коре он содержится в виде оксидов тех или инных элементов. Следует заметить, что кислород является неотъемлемой частью жизни на нашей планете. Почти каждому живому организму на планете нужен кислород для дыхания. Свободный кислород в природе вырабатывают зеленые растения. Причем это не только трава, деревья и кустарники, а так же зеленые водоросли мирового океана. Некоторые источники утверждают, что зеленые водные водоросли вырабатывают до 75% свободного кислорода на нашей планете. Подведя итог, можно утверждать, что кислород «приложил руку» ко всему на нашей планете, что мы можем наблюдать.
Применение кислорода
Кислород применяется в разных областях деятельности. Самыми популярными областями применения кислорода являются медицина, военное дело и промышленность. Большая часть всего произведенного промышленного кислорода расходуется на изготовление стали из железной руды. В этом направлении расходуется около 55% всего кислорода. Вторым по применению кислорода идет медицина. Тут стоит отметить многочисленные лекарственные препараты и процедуры в составе которых необходим кислород. Если взять лекарственные препараты — то это почти все жидкие лекарства. В пример можно самую известную жидкость — перекись водорода. Что же касается процедур, то тут также можно привести в пример элементарное — кислородная терапия. Эта процедура используется при лечении эмфиземы, пневмонии и некоторых сердечных заболеваний.
Следующей значимой областью применения является военное дело. Тут можно отметить, что чистый кислород используется в качестве окислителя в ракетном топливе. Так же значительную часть промышленного кислорода используется для поддержания жизнеобеспечения в тяжелых условиях. В пример можно поставить дайверов, космонавтов и покорителей горных вершин. Еще кислород находит применение в сварке, очистке воды и химической промышленности. Доля которого составляет около 25% от общего объема.
Интересные факты
Урок 11 Бесплатно Кислород
Кислород – химический элемент и простое вещество
Кислород – самый распространенный на Земле химический элемент:
земная кора содержит 47% кислорода
мировой океан состоит из кислорода на 85%
Кроме этого, кислород – основной участник обмена веществ в живых организмах – дыхания и фотосинтеза.
В таблице приведены основные сведения о кислороде.
Химический элемент
Простое вещество
Название «Oxygenium» произошло от двух слов, в переводе «рождающий кислоты»
Химический знак – О
Атомный номер – 8
Расположение в периодической системе – 2 период, VI группа
Типичный неметалл (сильный окислитель)
Атомная масса – 16 а. е. м.
Степени окисления – –2; 0; +1; +2
Химическая формула – O2
Молекулярная масса – 32 а. е. м.
Бесцветный газ без запаха; светло-голубая жидкость; синие кристаллы
Температура кипения – –183 °С
Температура плавления – –218 °С
В жидком состоянии кислород имеет голубой цвет, поэтому на всех формулах мы его будем обозначать голубым!
Изучением кислорода занимались несколько учёных примерно в одно и то же время.
Официально первооткрывателем кислорода считается англичанин Джозеф Пристли (1774 год).
Однако установлен факт, что в свое время Леонардо да Винчи изучал химию кислорода, не подозревая тогда, что он является элементом.
Название «кислород» в русский язык ввёл Михаил Ломоносов, который также ввёл в употребление термин «кислота», который в те времена обозначал оксид – соединение элемента с кислородом.
Поэтому истинное значение названия «кислород» переводится как «рождающий оксиды». Некоторое время в России кислород называли «кислотвор».
Химический элемент кислород образует два простых вещества: кислород (O2) и озон (O3).
Кислород активно участвует в обмене веществ, именно ему обязана наша планета возникновением на ней жизни.
Атмосфера содержит 21 % кислорода.
Считается, что несколько сотен миллионов лет назад концентрация кислорода в атмосфере была почти в 2 раза выше – около 40%.
Количество кислорода в воздухе ниже 8% является угрозой для жизни человека.
В отличие от кислорода, озон даже в газообразном состоянии имеет голубой цвет, в жидком – насыщенный фиолетовый, в твёрдом – почти чёрный.
Озон (O3) образуется из кислорода при воздействии ионизирующих излучений: радиации или жестких ультрафиолетовых лучей (это свойство кислорода было открыто в 1899 году учеными Пьером и Марией Кюри).
Он образуется в атмосфере под воздействием разрядов молнии, а также при работе бытовой техники, например, лазерных принтеров.
При этом вы можете чувствовать характерный запах – это и есть запах озона.
Слово «озон» с греческого языка так и переводится: «пахну».
Озон также способен в некоторой степени задерживать ультрафиолетовые лучи. Это его свойство является одним из факторов существования жизни на Земле.
Кислород и озон являются парамагнетиками – это значит, что они притягиваются к магниту.
Это заметно при проведении опытов с жидкими кислородом и озоном.
Пройти тест и получить оценку можно после входа или регистрации
Химические свойства кислорода
Существует два способа получения кислорода:
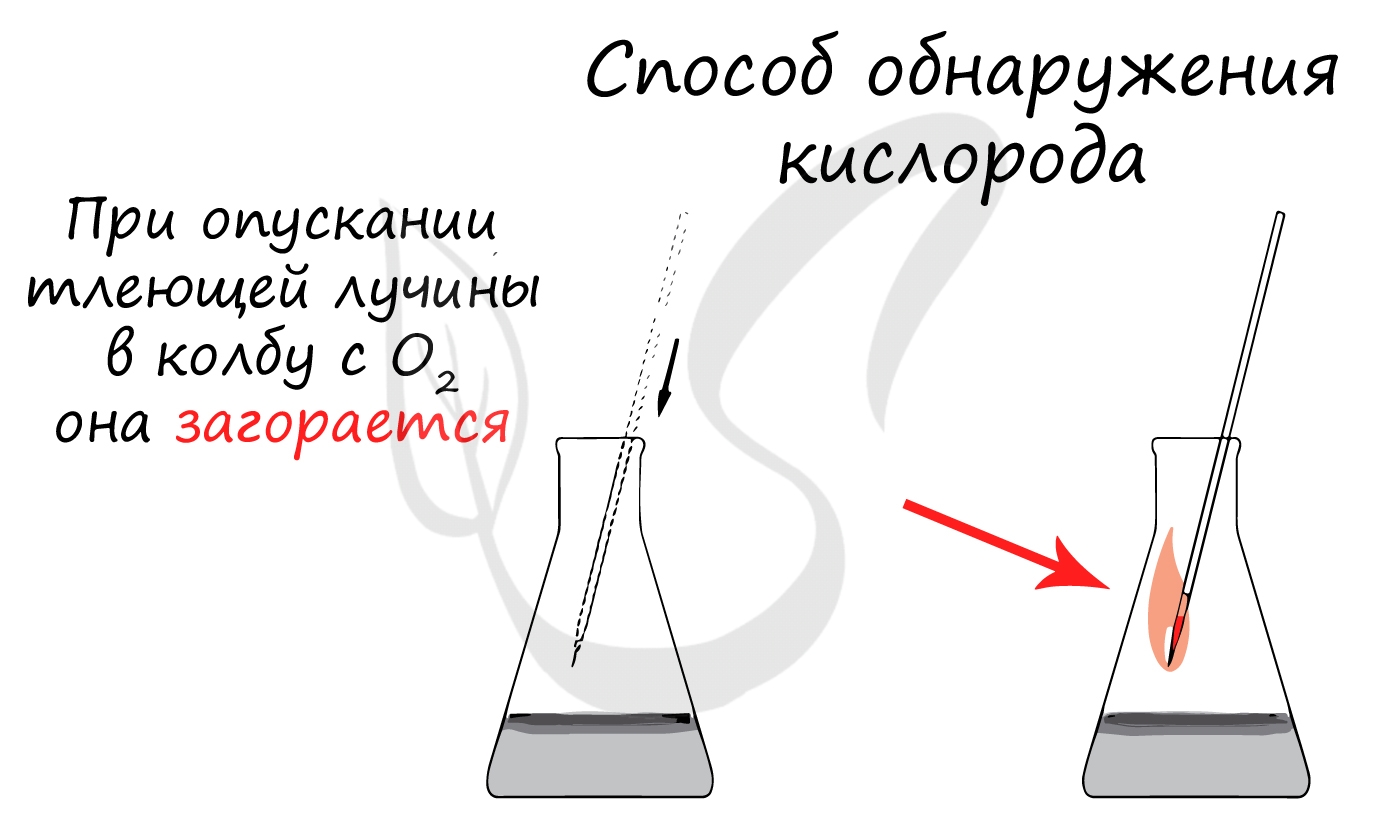
Качественной реакцией на кислород является его способность зажигать тлеющую лучину.
Кислород – очень активное вещество, при нормальных условиях он взаимодействует почти со всеми простыми веществами, кроме нескольких.
В чистом кислороде горят даже на первый взгляд негорючие материалы, например, железо.
У меня есть дополнительная информация к этой части урока!
Этот эксперимент вы можете провести и в бытовых условиях.
Только проводить этот опыт надо, предварительно договорившись со взрослыми, и обязательно под их контролем!
Помните: любой химический эксперимент всегда таит в себе множество опасностей! Поэтому присутствие взрослого человека обязательно!
Возьмите небольшое количество (около 5 мл) пероксида водорода в стеклянном стаканчике и всыпьте в него перманганат калия (марганцовку) на кончике ножа.
Помните, что перманганата калия требуется минимальное количество, а также то, что в ходе этой реакции выделяется большое количество тепла!
Теперь, если внести в стакан почти погасшую лучину (спичку), то она ярко вспыхнет.
Поэтому делать это нужно аккуратно, лучше взять лучину подлиннее.
Реакции взаимодействия веществ с кислородом называются реакциями окисления.
Сложные вещества, состоящие из атомов двух химических элементов, один из которых – кислород, называются оксидами.
В этом правиле есть единственное исключение: соединения кислорода и фтора называются фторидами кислорода, поскольку окислителем («отнимающим электроны») здесь является не кислород, а химически более активный фтор.
Многие оксиды имеют собственные («тривиальные») названия.
Наиболее часто встречающиеся нам в обыденной жизни оксиды приведены в таблице.