Как вылечить клебсиеллу у грудничка
Коррекция острых и персистирующих форм клебсиеллезной инфекции у детей.
Рябчук Ф.Н., Пирогова З.И.
Клебсиеллы – грамотрицательные неподвижные капсульные палочки, при выращивании на питательных средах продуцируют слизистые колонии. Источником инфекции является больной человек или носитель. Возбудитель передается фекально-оральным и воздушно-капельным путем. Клебсиеллы продуцируют энтеротоксин, обладающий гемолитическим и эндотелиотропным действием, что вызывает гемодинамические нарушения в очагах поражения органов и тканей. Описаний течения острой инфекции, вызванной клебсиеллами у детей раннего возраста, в литературе приводится достаточно, но особенности течения клебсиеллеза у детей старшего возраста, в частности в ассоциации с другими УПМ при дисбактериозе, требуют дополнительного изучения.
Цель исследования. Сопоставить особенности течения клебсиеллезной инфекции у детей раннего и старшего возраста и оценить параклинические показатели исследований, в том числе результаты общей иммунологической реактивности у детей при остром и персистирующем течении клебсиеллеза.
Материал и методы. Обследовано 60 детей младшего и старшего возраста с бактериологическим высевом клебсиелл из кишечника. В комплекс исследований включались оценка анамнеза, клинического статуса, анализа крови, копроцитограммы, УЗИ органов брюшной полости, фиброгастродуоденоскопия (по показаниям), микробиологический анализ кала на дисбактериоз, бактериологические посевы кала на патогенную кишечную инфекцию, ИФА на ротавирус, посев кала на клебсиеллезную флору на селективную среду. Оценивались интегральные показатели общей иммунологической реактивности: коэффициент фагоцитарной защиты (КФЗ), иммунный лимфомоноцитарный потенциал (ИЛМП) и лейкоцитарный индекс интоксикации (ЛИИ).
Результаты. Под наблюдением находилось 60 детей с клебсиеллезной инфекцией в возрасте от 1 месяца до 10 лет. Детей первого года жизни было 34, от 1 года до 7 лет – 21, старше 7 лет – 5. Течение клебсиеллезной инфекции было острым у 22 детей (1 группа), персистирующим – у 38 больных (2 группа). Клинические признаки острого течения клебсиеллеза были у детей 1 группы и отмечались ярко очерченным бурным началом болезни с лихорадкой до 39,10С (у 5 детей – 22,8%), появлением рвоты от 3 до 5 раз в сутки у 18 детей и полным отказом от еды у 4 детей (82% и 18% соответственно). Стул был жидким с частотой до 5 раз в сутки у 12 детей (54,5%) и до 7-10 раз/сутки – у 10 детей (45,5%), в стуле была примесь слизи, зелени, у 2 детей были прожилки крови.
У детей 1 группы в копроцитограмме были признаки острой воспалительной реакции в кишечнике: отсутствие детрита, слизь, лейкоциты до 15-35 в поле зрения или скопления лейкоцитов на слизи, кишечный эпителий и единичные эритроциты. В гемограмме у больных был выраженный лейкоцитоз (в среднем 13,2*109/л±1,0), нейтрофилез со сдвигом влево (48±3,54% при возрастной норме – 30%), ускоренная СОЭ (в среднем – 18,6±1,64 мм/час), анэозинофилия (у 20 больных из 22 детей 1 группы, то есть у 90,9% пациентов). Бактериологические посевы на патогенную кишечную флору и ИФА на ротавирус были негативными. В посевах испражнений у детей 1 группы (в 100% случаев) отмечался обильный рост клебсиелл в титре 108-1010. Штамм Kl. pneumoniae обнаруживался у 20 детей и только у 2 больных был рост Kl. oxytoca.
Показатели общей иммунологической реактивности у детей с острым течением клебсиеллеза характеризовались резко сниженными величинами как КФЗ, так и ИЛМП, они составили в среднем 0,465±0,04 и 0,440±0,06 при возрастной норме 0,792±0,02 и 0,745±0,02 (p
Краевое государственное бюджетное учреждение здравоохранения
ДЕТСКАЯ ГОРОДСКАЯ БОЛЬНИЦА
министерства здравоохранения Хабаровского края
Лечение дисбактериоза кишечника у детей
Какая мама согласится во время болезни своего малыша на то, чтобы ему антимикробные препараты кололи внутримышечно, а не просто давали бы микстуру или таблетку? Далеко не каждая. Абсолютно точно. А почему?
Преобладающее с огромным перевесом большинство скажет: «Чего я буду его травмировать, уколы делать. когда так удобно – в ложечке микстуру дать». И не задумываются мамы, насколько серьезными могут быть последствия таких необдуманных поступков. Хотя, почему сразу антибиотики? Есть масса других заболеваний, состояний и лекарств, вызывающих эту проблему. И не только у детей.
Дисбактериоз. О нем и стоит поговорить в виду множественных эпидемий различных заболеваний, а также в связи с огромным ростом фармацевтической промышленности.
Что же такое «микрофлора» и «дисбактериоз»?
Кишечник Ни для кого из читателей не секрет, что в нашем организме «проживает» огромное количество микроорганизмов, их более 490 видов. Но далеко не все они способны и будут вызывать различные заболевания. Поэтому существует патогенная и условно-патогенная микрофлора. Вообще, у каждого человека есть свое «население», свои микроорганизмы, которые поддерживают в свою очередь сам организм. То есть это своеобразный симбиоз: «ты – мне, я – тебе».
В разных отделах пищеварительной системы находятся разные «поселенцы». Так, например, во рту (между прочим, самом «густонаселенном» месте нашего организма) и в толстом кишечнике преобладают анаэробы (кишечная палочка, энтеробактерии, дрожжеподобные грибы); а желудок вообще «беден», т.к. в соляной кислоте многие не выживают.
Зачем они нужны? Пища, которую мы употребляем, может быть очень полезной, но в той форме, в которой она попадает в желудок, наш организм ее не усвоит. Значит, нужно как-то ее «обработать» и «подать». Для этого и нужен весь состав микрофлоры. И здесь главную роль играют облигатные микроорганизмы.
Облигатные микроорганизмы – это главная, постоянная микрофлора. Она начинает формироваться с первого в жизни кормления малыша и стабилизируется к 2 месяцам.
Далее в течение жизни происходит постепенное заселение кишечника условно-патогенной микрофлорой. Ее необходимость до конца не доказана. Одни врачи считают, что при наличии их в кишечнике снижается риск общей заболеваемости кишечными инфекциями, повышается иммунитет. Другие считают наоборот, что это вызывает большую заболеваемость. В любом случае – условно-патогенные микроорганизмы есть, есть всегда.
Условно-патогенная микрофлора – это второстепенные «поселенцы», которые могут находиться в организме длительное время, не причиняя никакого вреда. Но если в кишечник попадает большое количество бактерий такого же рода, либо резко снижается иммунитет, заболевание манифестирует в тяжелой форме. В здоровом организме же рост этой микрофлоры сдерживают облигатные микроорганизмы.
И третья, наиболее опасная группа микроорганизмов – это патогенные, т.е. болезнетворные.
Патогенная флора в организме человека не существует постоянно. А, поступая из вне, вызывает заболевание либо путем разрушения нормальной микрофлоры, либо очень быстрой персистенцией (размножением и заселением). Почти сразу или на фоне сниженного иммунитета и угнетенных защитных сил организма.
Таким образом, первые две группы существовать в кишечнике могут и существуют. Появление же представителей третьей группы микроорганизмов вызывает разбалансировку, дисбаланс всей микрофлоры. Облигаты погибают, что усиливает рост патогенных штаммов. появляются клинические признаки этого дисбаланса. Это и называется дисбактериозом.
Факторы, влияющие на состав микрофлоры кишечника
Так как речь пойдет о нарушении самой микрофлоры у ранее здорового малыша, рассматривать случаи попадания патогенных микроорганизмов извне мы не будем.
Итак, причины такого нарушения, дисбаланса микрофлоры можно разделить на внешние и внутренние.
Внешние причины:
Внутренние причины:
Итак, разобравшись с основными большими группами причин возникновения дисбактериоза, можно попытаться распознать дисбактериоз.
Как понять, что нужна помощь?
Самым простым способом выявления дисбактериоза у детей является копрология – исследование кала Важно помнить, что у маленьких детей дисбактериоз отличить от физиологически нормально протекающих процессов довольно сложно. Поэтому важную роль играют «предшественники». Допустим, мама знает, что ее малыш недавно переболел пневмонией, при которой применялись антибиотики, но профилактику дисбактериоза в виде далее описанных препаратов не проводили. Конечно, в этом случае, будем думать именно о дисбактериозе. То же самое касается любых выше названных состояний, при которых возможно его возникновение.
Итак, самым простым способом является копрология – исследование кала. Здесь в первую очередь смотрим, насколько поступившая пища усвоилась организмом. Если в анализе много непереваренных мышечных волокон, жирных кислот, клетчатки, крахмала, значит, пищу организм усваивает плохо. И одной из причин является нарушение в микрофлоре и что-то, что не позволяет ей «работать». Это и возможно при дисбактериозе, когда патогенные микроорганизмы подавляют облигатную флору. Также в анализе зачастую встречается большое количество лейкоцитов и клеток кишечного эпителия, которые появляются в нем за счет воспаления кишечной стенки, оставшейся без своих микроорганизмов. Ну и конечно, цвет и консистенция каловых масс сами дадут знать о нарушениях в организме – стул жидкий, обильный, частый, с большим количеством воды, чаще светлого цвета. При этом малыш будет постоянно просить пить, и в тяжелых случаях может развиваться эксикоз – обезвоживание. Самые маленькие детки перестанут прибавлять в весе, даже начнут худеть. Кожа становится сухой, теряется ее эластичность.
Конечно, в таких случаях дети нуждаются в госпитализации и срочной коррекции состояния. Мы же поговорим о нетяжелых вариантах дисбактериоза кишечника после, например, приема антибиотиков.
Лечение дисбактериоза
Ключевым моментом в лечении дисбактериоза является коррекция питания Первым и ключевым моментом в лечении дисбактериоза является коррекция питания. Итак, обращаю внимание читателей на продукты, которые следует исключить из рациона во избежание раздражения слизистой оболочки желудочно-кишечного тракта и усиления перистальтики. Это делается с целью сохранить воду в организме.
А именно, прекращаем употреблять в пищу сырые овощи, фрукты, за исключением бананов и печеных яблок. Из мясного допускается нежирная курица, кролик, крупы – рисовая, манная (если нет аллергии), пшенная. Причем все каши употребляем в протертом виде. Хорошо пить просто рисовый отвар. Из овощей оставляем только картошку. Молочные продукты исключаем полностью. Из напитков позволительны чай крепкий, сладкий, вода, компот из сухофруктов (причем только сам компот без ягод), отвар ромашки, кисели. Соки и газированные напитки – категорически нельзя.
Часто для лечения дисбактериозов у детей применяют бактериофаги. Это вирусы бактерий, которые избирательно убивают причину возникновения дисбактериоза. Но их применение возможно лишь после доподлинно известного возбудителя.
Пробиотики. На сегодняшний день это самая разнообразная и часто используемая группа препаратов для лечения дисбактериозов у детей. Название говорит само за себя – «для жизни» (антибиотики – «против жизни»). Принцип их действия заложен в них самих – молочнокислые бактерии «встают на защиту» кишечника и подавляют микроорганизмы, вызывающие процессы гниения.
Пребиотики являются стимуляторами пробиотиков. Ну а симбиотики – это комплексные препараты, включающие в себя как пре-, так и пробиотики. Рассмотрим наиболее часто применяемые из них:
Аципол обладает многофакторным действием, высокоактивен, а также повышает иммунологическую резистентность организма.
Применяют: у детей до 6 месяцев 5 доз в сутки, старше 6 месяцев 10-15 доз в сутки в 2-3 приема за 30-40 минут до еды. Препарат растворяют в воде комнатной температуры из расчета одна чайная ложка на одну дозу препарата.
Линекс стабилизирует мембраны клеток кишечного эпителия и регулирует всасывание электролитов.
Применяют: у детей до 2 лет по 1 капсуле 3 раза в сутки; старше 2 лет по 1-2 капсуле 3 раза в сутки. Детям раннего возраста капсулу вскрывают и смешивают с небольшим количеством жидкости. Курс 5-7 дней.
Энтерол, активным компонентом которого являются лечебные дрожжи, устойчивые ко всем видам антибиотиков.
Применяют: у детей до года по пол пакетика 2 раза в сутки, у детей от 1 до 3 лет по 1 капсуле или 1 пакетику 1-2 раза в сутки, старше 3 лет по 2 капсулы или 2 пакетика 1-2 раза в сутки за 30 минут до еды.
Бифидумбактерин восстанавливает активность ЖКТ, подавляет рост патогенной микрофлоры, повышает иммунный статус.
Применяют: у детей до 6 месяцев по 5-10 доз в сутки; с 6 месяцев до 3 лет – по 1-15 доз в сутки; старше 3 лет – по 15-20 доз в сутки на 2-3 приема за 30 минут до еды.
Бифилин имеет более широкий спектр ферментативной активности по сравнению с бифидумбактерином.
Применяют: у детей старше 3 лет по 10-12 доз в сутки в 2-3 приема за 30 минут до еды. Для растворения препарата используют кипяченую воду из расчета 1 доза препарата на 1 чайную ложку.
Бифиформ Малыш содержит помимо лакто- и бифидобактерий витамины В1 и В6.
Применяют: у детей от 1 года до 3 лет по 1 порошку 2-3 раза в сутки, таблетки жевательные детям 2-3 лет по 1 таблетке, с 3 лет по 2 таблетке 2-3 раза в сутки независимо от приема пищи. Курс 5 дней.
Бифиформ выпускается в капсулах, которые устойчивы к желудочному соку, благодаря которым бактерии доходят до кишечника в неизмененном виде.
Применяют: у детей старше 2 лет по 1-2 капсуле 2 раза в сутки независимо от приема пищи. Курс 10-14 дней.
В настоящее время широко используются продукты, содержащие бифидо- и лактобактерии. Наиболее широко используются: Бифидок, Бифилин, кисломолочный бифидумбактерин, Биолакт обогащенный, Имунеле, Активиа, Актимель и т.д.
Единственный их минус – сроки хранения некоторых продуктов напрямую зависят от содержания полезных бактерий. То есть чем больше срок их хранения, тем меньшее количество бактерий в них содержится.
Симптомы клебсиеллёзов
В летний период становятся актуальны заболевания вызванные инфекционными агентами.
Особенно активны микроорганизмы семейства энтеробактерий – грамотрицательные, палочкообразные, с жгутиками для передвижения и прикрепления, факультативные анаэробы: кишечная палочка, сальмонелла, клебсиелла и др. Так, клебсиелла – klebsiella, может существовать в почве, воде, месяцами оставаясь жизнеспособной, сохраняется на пище и пыли.
Клебсиеллы могут попасть в организм через желудочно-кишечный тракт, с плохо вымытых рук, овощей и фруктов, с водой, с почвой. Однако, этот микроорганизм входит в группу условно-патогенной микрофлоры и определяется у абсолютно здоровых детей и взрослых, считается одним из элементов нормальной флоры кишечника.
При этом, клебсиелла является одной из самых распространённых внутрибольничных инфекций, т.к. она устойчива к действию факторов окружающей среды, высоким температурам. Хотя, за несколько минут она гибнет от дезинфектантов, а при очень высоких температурах через 1-1,5 часа. При несоблюдении надлежащих правил гигиены, санитарных норм в помещениях, встречаются случаи заражения новорожденных клебсиеллой в роддомах. Малыш постоянно плачет и не может заснуть, его беспокоят колики и частый понос. А причина — клебсиелла – бактерия, устойчивая к губительному действию внешней среды, покрытая плотной капсулой.
Факторы развития клебсиеллеза
Клебсиеллы относятся к одному семейству с бактериями рода Serratia и Enterobacter. Этими возбудителями, особенно Serratia, обладающий наибольшей лекарственной устойчивостью, обусловливаются вспышки инфекции в стационарах, в связи с загрязнением ряда медикаментозных средств, лекарственных растворов, применяемых в терапии органов дыхания. Их трудно, но можно дифференцировать только с помощью специальных проб. Klebsiella Enterobacter и Serratia, вызывающие внутрибольничную пневмонию, инфекцию мочевого тракта, бактериемию, обладают различной чувствительностью к противомикробным препаратам.

Если защита организма человека по какой то причине ослаблена: снижен общий иммунитет, часто грипп, ОРВИ, применение антибиотиков, употребление загрязненных, некачественных продуктов, сахарный диабет, алкоголизм и др., клебсиелла начинает активно размножаться, выделять токсины, вызывая эндотоксимию и воспалительные процессы в разных органах. Развиваются такие заболевания, как воспаление легких, воспалительные заболевания мочевыводящих путей, менингит, конъюнктивит, кишечные инфекции, сепсис и достаточно редкие болезни – озена (зловонный насморк), риносклерома.
Наиболее часто клебсиелла вызывает пневмонию и поражение кишечника. У взрослых людей чаще встречается пневмония, вызванная палочкой Фридлендера. В связи с особенностью иммунитета новорожденных и недостаточностью у них нормальной микрофлоры на коже, в дыхательных путях и особенно в кишечнике — клебсиелла — Klebsiella oxytoca — чаще вызывает поражения желудочно-кишечного тракта — толстого кишечника.
Симптомы клебсиеллы (клебсиеллёза) в ЖКТ у грудничков
Симптомы клебсиеллы у малышей схожи с симптомами дисбактериоза: вздутие, метеоризм, колики, срыгивание. Но чаще проявляются — жидким стулом со слизью, кровью и резким запахом, повышением температуры, лихорадкой, болями в животе и сильным обезвоживанием организма. В зависимости от того, какой иммунитет у малыша, течение заболевания может протекать как в лёгкой форме, так и грозить тяжелыми инфекционными осложнениями. Если клебсиелла в организме быстро размножается, выделяет токсины, нарастает интоксикация, обезвоживание, то заболевание может проявиться в течение нескольких часов и потребует срочной госпитализации ребенка.
Поэтому, при любом расстройстве стула, необходимо обратиться к врачу, сдать кал ребёнка на анализ, пройти обследование, чтобы точно выявить, какие именно бактерии вызвали изменение состояния ребёнка. Большую роль в восстановлении иммунитета и нормальной микрофлоры у новорожденного играет грудное вскармливание. При высокой обсеменённости клебсиеллой и тяжёлой форме заболевания, лечении ребенка в больнице, назначают сложную терапию с применением антибиотиков. Если заболевание грудничка протекает в лёгкой форме, то для коррекции микрофлоры кишечника назначают пробиотики. Синбиотики – Нормофлорины Л и Б – обладают активным противовоспалительным, антисептическим и питательным действием, что важно при клебсиеллёзной инфекции. Ребенок может чувствовать себя нормально, а при обследовании находят в анализах повышение количества клебсиелл. Тогда препараты с лакто- и бифидобактериями назначают для вытеснения излишнего количества клебсиеллы, повышения иммунитета, улучшения собственной полезной микрофлоры.
Симптомы клебсиеллы в других органах и системах
Если клебсиеллы попадают в мочевыделительную систему, то они способны вызывать уретрит, пиелонефрит, со стойким рецидивирующим течением, плохо поддающимся терапии и часто измененной чувствительностью к антибиотикам. В редких случаях клебсиеллёза, возможно такое осложнение, как – озена — зловонный насморк, с поражением слизистой носа, образованием гнойных, болезненных, кровоточащих корок.
Симптомы и признаки инфекций мочевыводящих путей, желчного пузыря и в брюшной полости, вызываемых клебсиеллами, не отличаются от симптоматики, обусловленной кишечной палочкой. Развиваются они чаще у больных сахарным диабетом и у пациентов, получающих антимикробные препараты, к которым устойчив возбудитель заболевания. Клебсиелла является также важным этиологическим фактором септического шока.
Клебсиелла известна как фактор развития легочных заболеваний, однако, среди причин, вызывающих бактериальную пневмонию, имеет около 1% всех случаев. Встречается преимущественно у мужчин в возрасте старше 40 лет, с хроническими бронхолегочными заболеваниями, больных сахарным диабетом и лиц с алкоголизмом. У пожилых людей, грамотрицательные бактерии заселяют ротоглотку и могут распространиться по дыхательному тракту, вызывая пневмонию или гнойный бронхит.
Клинические симптомы клебсиеллёзной пневмонии сходны с проявлениями при пневмококковой пневмонии, но чаще характеризуются более тяжелым течением: внезапным началом, ознобов, стойким повышением температуры тела, продуктивным кашлем, иногда с прожилками крови и резким запахом, с сильными плевральными болями, появлением одышки. Больные часто находятся в прострации и бредовом состоянии, за счет интоксикации. Чаще всего очаг воспаления располагается в правой верхней доле легкого, но может быстро прогрессировать, если лечение не проводится и распространиться с одной доли на другую. Появляются цианоз и одышка, могут возникнуть желтуха, рвота, диарея. Выявляется, при обследовании, образование плеврального выпота, уплотнение легочной ткани, или некротизирующая пневмония, с быстрой кавернизацией. На фоне интоксикации определяется снижение количества лейкоцитов в периферической крови, а не повышение, как при воспалении. Гораздо чаще наблюдаются абсцессы и эмпиемы легких. Это объясняется способностью клебсиелл вызывать деструкцию ткани. Не всегда выявляются характерные признаки при рентгеновском обследовании: уменьшение объема легкого, его уплотнение, эмфизематозные изменения. При медленном прогрессировании инфекционного воспалительного процесса может развиться хронический некротизирующий пневмонит, напоминающий туберкулез, с продуктивным кашлем, слабостью, выраженной анемией.
Лечение клебсиеллезов
Лечение заболеваний, вызванных клебсиеллой, зависит от локализации и выраженности патологического процесса. Антибиотики назначают в тяжелых случаях по чувствительности, при легком течении или только обнаружении в анализах повышения клебсиелл — не применяют. Обязательно используют разнообразные препараты, восстанавливающие кишечную микрофлору.
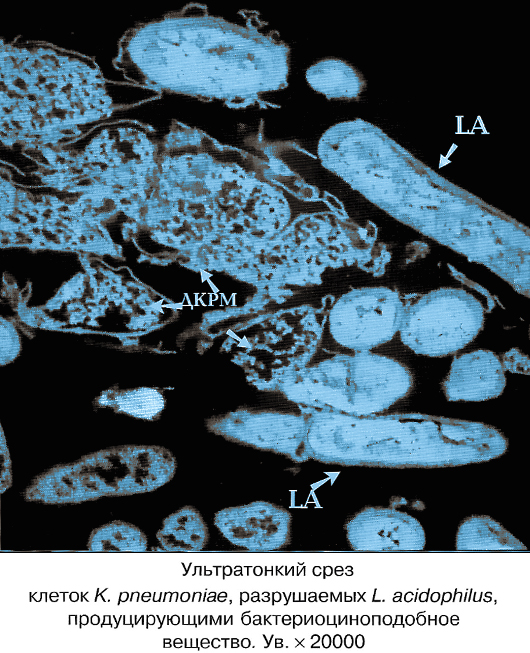
Как правило, антимикробную терапию рекомендуют начинать еще до получения результатов посева и определения лекарственной чувствительности к антибиотикам. В этом случае биокомплексы Нормофлорины, содержащие продукты жизнедеятельности живых лакто- и бифидобактерий с активным антисептическим, противовоспалительным действием, оказывают лечебный эффект при клебсиеллёзах, что доказано научными исследованиями и многолетней практикой, как у новорожденных, беременных, кормящих, так и взрослых и пожилых.
К вопросу о дисбиозе кишечника и его коррекции у детей
Важнейшую роль в жизнедеятельности организма человека играет микробиоценоз кишечника. Всю микрофлору кишечника можно разделить на три группы: основная — бифидобактерии ( Bifidobacterium (В.) bifidum, B. brevis, B. longum, B. adolescentis и др.) и лактоба
Нормальная микрофлора выполняет важные функции — защитную, обменную и иммуноиндуцирующую, участвуя в поддержании гомеостаза. Нарушение любой из них сопровождается изменением метаболизма, возникновением дефицита микронутриентов, снижением иммунного статуса.
Нарушения микробиоценоза кишечника связаны с характером питания, возрастом, проведением антибактериальной, гормональной, лучевой терапии, хроническими заболеваниями желудочно-кишечного тракта, изменением иммунного статуса, состоянием окружающей среды; они наступают задолго до клинических проявлений. Изменения нормальной микрофлоры получили название дисбактериоза, или дисбиоза. Дисбактериоз является микробиологическим понятием и ни в коем случае не может быть самостоятельным диагнозом.
Микроэкологическая классификация степеней тяжести дисбиоза кишечника была предложена в 1998 г. С. Д. Митрохиным.
I степень тяжести — увеличено или уменьшено общее количество кишечных палочек. Кишечные палочки с атипичными биологическими свойствами отсутствуют. Количество бифидобактерий и лактобацилл не изменено. Изменения в общих показателях микробного метаболитного паспорта фекалий характерны лишь в отношении пула летучих жирных кислот (ЛЖК), содержания фенилпропионовой кислоты, скатола и метиламина. Общее содержание ЛЖК у больных с I степенью тяжести дисбактериоза может быть несколько меньшим или большим, чем у здоровых лиц. Содержание скатола снижено. Содержание фенилуксусной кислоты и метиламина повышено. Отмечаются изменения удельного веса щавелевоуксусной кислоты в профиле дикарбоновых кислот (ДКК). Дисбактериоз — латентный, компенсированный, кишечные дисфункции не регистрируются.
II степень тяжести — незначительно снижено количество бифидобактерий и лактобацилл. Наблюдаются количественные и качественные (появление форм с атипичными биологическими свойствами) изменения кишечных палочек. Высеваются в умеренном количестве условно-патогенные кишечные микроорганизмы. Отмечаются изменения как в общих, так и в специфических показателях микробного метаболитного паспорта фекалий (снижение экскреции с фекалиями фенольных соединений: п-крезола, индола, а также скатола). Количество фенилпропионовой кислоты на порядок превышает таковое у здоровых лиц. Профиль фенольных соединений (ФС) также меняется: удельный вес индола возрастает более чем в 2 раза, несколько снижается удельный вес п-крезола и более чем в 10 раз снижен удельный вес скатола. В целом экскреция с фекалиями карбоновых и ароматических аминокислот, фенольных и индольных соединений (за исключением фенилаланина), а также гистамина и серотонина при II степени тяжести дисбиоза снижена. Изменен профиль сложных и простых аминов (АмП): удельный вес гистамина и серотонина ниже, а представителя простых аминов — метиламина — выше. Дисбактериоз — локальный (местный), субкомпенсированный; кишечные дисфункции, как правило, не наблюдаются.
III степень тяжести — существенное снижение количества бифидобактерий (105–106) в сочетании со снижением количества лактобацилл и резким изменением типичных свойств кишечных палочек (значительное преобладание гемолитических, лактозонегативных форм). Значительное увеличение количества условно-патогенных бактерий с патогенными свойствами (гемолитических форм) и патогенных дрожжеподобных грибов (родов Candida albicans, Geotrichum и др.). Характерны еще более выраженные изменения как в общих, так и в специфических показателях микробного метаболитного паспорта фекалий. Снижена величина экскреции с фекалиями ФС: п-крезола и индола. В фекалиях практически отсутствует скатол. Напротив, содержание фенилпропионовой кислоты в каловых массах резко увеличивается. Профиль ФС меняется таким образом, что существенно увеличивается удельный вес индола и значительно снижается удельный вес п-крезола. Cодержание в фекалиях гистамина и серотонина может быть выше или ниже по сравнению с нормой (зависит от нозологической формы основного заболевания). Содержание карбоновых кислот меняется следующим образом: резко уменьшается пул ЛЖК, практически не обнаруживается щавелевоуксусная кислота и значительно возрастает экскреция с каловыми массами альфа-кетоглутаровой кислоты. Изменен профиль ЛЖК. При нарушениях стула по типу диареи удельный вес уксусной кислоты ниже, а пропионовой и масляной кислот, наоборот, повышен, при констипации наблюдается противоположная картина. Отмечаются снижение или увеличение удельного веса молочной кислоты и аналогичные изменения удельного веса альфа-кетоглутаровой кислоты в профиле ДКК.
IV степень тяжести — резкое снижение или отсутствие бифидобактерий, значительное уменьшение количества лактобацилл, резкое уменьшение количества или отсутствие кишечных палочек с типичными свойствами, значительное возрастание количества как облигатных, так и факультативных видов (в норме не встречающихся) кишечных бактерий и дрожжеподобных грибов с патогенными свойствами. Выявляются патогенные кишечные бактериии (сальмонеллы, шигеллы, ерсинии). Качественные изменения в микробном метаболитном паспорте остаются такими же, как и при III степени, но их количественные характеристики еще более изменены; характерна глубокая разбалансировка биохимических регуляторных механизмов микробной экосистемы, сочетающаяся с аналогичной разбалансировкой микробной инфраструктуры кишечника. Дисбактериоз — распространенный (с бактериемией), декомпенсированный (с угрозой генерализации инфекции, сепсиса или септикопиемии); наблюдаются выраженные кишечные дисфункции.
В клинической практике условно выделяются три основные группы кишечной микрофлоры: облигатная — постоянно встречающаяся (резидентная, аутохтонная, индигенная); добавочная (сопутствующая) и транзиторная (случайная, аллохтонная) (табл.).
В зависимости от клинических проявлений выделяют различные степени проявления дисбактериоза. В частности, одна из таких классификаций принадлежит В. А. Таболину (1998).
I степень — латентная фаза дисбиоза, проявляется только в снижении на один-два порядка количества защитной микрофлоры — бифидобактерий, лактобацилл, а также полноценных кишечных палочек (до 80% от общего количества). Остальные показатели соответствуют физиологической норме (эубиозу). Как правило, начальная фаза не вызывает дисфункций кишечника и возникает при воздействии неблагоприятных факторов (нарушение режима питания и др.). В этой фазе возможно вегетирование в кишечнике незначительного количества отдельных представителей условно-патогенной флоры. Клинических проявлений дисбактериоза в этой фазе нет.
II степень — пусковая фаза более серьезных нарушений, характеризуется выраженным дефицитом бифидобактерий на фоне нормального или сниженного количества лактобацилл или снижения их кислотообразующей активности, дисбалансом в количестве и качестве кишечных палочек, среди которых нарастает доля лактозонегативных или цитратассимилирующих вариантов. При этом на фоне дефицита защитных компонентов кишечного микробиоценоза происходит размножение либо плазмокоагулирующих стафилококков, либо протеев, либо грибов рода Candida albicans. Вегетирование в кишечнике протеев или плазмокоагулирующих стафилококков в этой фазе развития дисбактериоза чаще транзиторное, чем постоянное. Функциональные расстройства пищеварения выражены неотчетливо — спорадически жидкий стул зеленоватого цвета с неприятным запахом, со сдвигом рН в щелочную сторону, иногда — задержка стула; может отмечаться тошнота.
III степень — фаза агрессии аэробной флоры, характеризующаяся отчетливым нарастанием содержания агрессивных микроорганизмов; при этом размножаются до десятков миллионов в ассоциации золотистые стафилококки и протеи, гемолитические энтерококки; наблюдается замещение полноценных эшерихий бактериями родов Klebsiella, Enterobacter, Citrobacter и др. Эта фаза дисбактериоза проявляется дисфункциями кишечника с расстройствами моторики, секреции ферментов и всасывания. У больных отмечается учащенный разжиженный стул, часто зеленого цвета, ухудшение самочувствия, дети становятся вялыми, капризными.
IV степень — фаза ассоциативного дисбиоза, характеризующаяся глубоким разбалансированием кишечного микробиоценоза с изменением количественных соотношений основных групп микроорганизмов, изменением их биологических свойств, накоплением токсических метаболитов. Характерно вегетирование энтеропатогенных серотипов E. coli, сальмонелл, шигелл и других возбудителей острых кишечных инфекций. Возможно размножение клостридий. Эта фаза дисбиоза характеризуется функциональными расстройствами пищеварительной системы и нарушениями общего нутритивного статуса, дефицитом массы тела, бледностью кожных покровов, частым стулом с примесью слизи, зелени, иногда крови, с резким гнилостным или кислым запахом.
Для подтверждения диагноза необходимо провести следующее исследование:
Определение состава фекальной микрофлоры — наиболее доступный метод, однако он недостаточно информативен, поскольку отражает микробный состав лишь дистальных отделов кишечника. Важным диагностическим тестом синдрома избыточного бактериального роста является экскреторный дыхательный тест с идентификацией различных метаболитов, которые продуцируются с участием интракишечных бактерий (лактулозный тест с определением в выдыхаемом воздухе Н2). Последний для повседневной педиатрической практики представляется наиболее приемлемым. Газожидкостная хроматография позволяет оценить химические соединения, связанные с жизнедеятельностью нормальной микрофлоры. В ряде случаев целесообразно исследование липополисахаридов (ЛПС)-О-антигена и уровня энтеротоксинов. Для определения степени дисбактериоза можно пользоваться стандартным методом Р. Б. Эпштейн–Литвак и Ф. Л. Вильшанской (1969).
Коррекция нормального состава кишечной флоры должна быть комплексной и направленной в первую очередь на лечение основного заболевания, вызвавшего дисбаланс микрофлоры; необходим комплекс лечебно-охранительных мероприятий по общему оздоровлению организма ребенка в целом и на коррекцию его микрофлоры в частности.
Организация охранительного режима включает благоприятную психологическую атмосферу, длительное пребывание на свежем воздухе, более продолжительный сон, соответствующий режим питания.
Адекватное, сбалансированное питание в соответствии с возрастом ребенка при нормальном функционировании органов и систем предотвращает развитие дисбиозов. Наиболее важным мероприятием является естественное вскармливание детей грудного возраста. Идеальной пищей для новорожденного ребенка и детей первых месяцев жизни является молоко матери, которое больше всего подходит ее ребенку, так как имеет родственную связь с его тканями. Углеводы грудного молока (90% из них составляет β-лактоза) ферментируются посредством бифидобактерий в молочную кислоту, которая обеспечивает низкий уровень рН стула у детей. В литературе неоднократно отмечалось влияние естественного вскармливания на состояние микробиоценоза кишечника у детей раннего возраста. Так, состав микрофлоры мекония новорожденных, получавших грудное молоко, отличался низким содержанием аэробной микрофлоры, превалированием бифидофлоры над аэробной флорой и низким содержанием гнилостных бактерий (клостридии, бактероиды, род Proteus). При искусственном вскармливании рост бифидобактерий либо отсутствовал полностью, либо их содержание было резко снижено.
В настоящее время широкое распространение получает так называемое функциональное питание. Употребляются готовые пищевые продукты, в которые добавлены биопрепараты, антиоксиданты, каротиноиды, ферменты и другие субстраты. Для детей раннего возраста, находящихся на искусственном вскармливании, рекомендуются адаптированные смеси, обогащенные представителями микрофлоры: «Малютка», «Биолакт адаптированный», «Бифидок», «Бифилин», «Бифидолакт», «Бифилайф», «Виталакт» и др. Во многих случаях оправдывает себя применение сухой смеси «Лактофидус», содержащей бифидобактерии и стрептококки, и смеси «НАН» с бифидобактериями. Для выхаживания детей неонатального периода разработано функциональное питание в виде лиофилизированного грудного молока, обогащенного B. bifidum. Принимая во внимание, что одним из важнейших этапов выхаживания новорожденных в отделениях реанимации и интенсивной терапии является организация рационального вскармливания, недавно на кафедре неонатологии РГМУ был разработан новый вид функционального питания специально для вышеназванного контингента детей. Данный тип функционального питания представляет собой лиофилизированное грудное молоко, содержащее B. bifidum 791 в концентрации 10 8 КОЕ/мл (Ю. Г. Мухина, 2000). Функциональное питание не относится к категории лекарственных препаратов, используется для улучшения здоровья человека в целом.
Диета у детей с проявлениями дисбактериоза должна быть полноценной по калорийности и содержанию основных физиологических ингредиентов. Прием пищи необходимо осуществлять в одни и те же часы, желательно восстановить эндогенный биоритм пищеварения. Питание должно быть как можно более разнообразным. При этом желательно исключить или ограничить употребление продуктов, агрессивных в отношении аутофлоры, таких как макароны и вермишель из муки высшего сорта, консервы и полуфабрикаты из мяса, рыбы, бобовых, все виды свинины, баранины, печень, почки, мозги, тугоплавкие животные жиры, цельное и сгущенное молоко, сладкие йогурты, консервированные овощи и фрукты, сладости, лимонад, мороженое, шоколад. К группе рекомендуемых продуктов, стимулирующих рост индигенной микрофлоры кишечника, относятся чечевица, изделия из пшеницы, ржи, кукурузы, гречихи, проса, некоторые овощи — капуста, морковь, кабачки, тыква, артишок, топинамбур, свежие фрукты, неконсервированные фруктовые и овощные соки, орехи, мясо и рыба нежирных сортов, кисломолочные продукты, растительные жиры.
В комплексной диетотерапии больных дисбактериозами можно использовать и кобылий кумыс. Под его влиянием у больных уменьшаются гнилостные процессы в кишечнике, снижается количество гнилостных бактерий и улучшаются биологические свойства E. coli и других представителей индигенной микрофлоры. Е. А. Толмачевой разработана технология изготовления кумыса из коровьего молока, изучено его действие на кишечную микрофлору. Применение коровьего кумыса приводило к резкому уменьшению роста в кишечнике спороносных анаэробных бактерий, главным образом B. putrificus, B. perfringens и B. sporogenes.
Важное значение имеет также наличие в питании овощей, фруктов и растений, обладающих антимикробной активностью. Многие антибактериальные вещества, выделенные из растений, стимулируют иммунобиологические реакции организма, инактивируют бактериальные экзотоксины и гиалуронидазу.
Представляется уместным подчеркнуть, что только комплексная коррекция дисбиоза дает более выраженный стойкий клинический и микробиологический эффект. Одной из главных составляющих этого комплексного подхода является заместительная терапия.
Важнейшим методом терапии дисбиоценоза (дисбактериоза) кишечника является применение лекарственных средств биологического происхождения, способных регулировать равновесие микрофлоры кишечника. С целью ликвидации дефицита индигенной флоры используют пробиотики — препараты живых микроорганизмов (представителей индигенной микрофлоры кишечника), которые обладают способностью целенаправленно регулировать кишечную микроэкологию и восстанавливать эубиоз. Это кисломолочные бактерии, бифидобактерии, кисломолочные стрептококки.
Препараты-пробиотики на основе этих микроорганизмов широко используются в западноевропейских странах, Канаде и США в качестве пищевых добавок, а также в йогуртах и других молочных продуктах. Микроорганизмы, входящие в состав пробиотиков, непатогенны, нетоксигенны, сохраняют жизнеспособность при хранении. Пробиотики не считаются лекарственными препаратами, а рассматриваются как средства, благоприятно влияющие на состояние здоровья людей. В педиатрической практике получили широкое распространение такие пробиотики, как Бифидумбактерин, Лактобактерин, Колибактерин, Бификол, Бифидумбактерин-форте, Ацилакт, Примадофилюс, Линекс, Бифиформ и др.
Линекс — комплексный препарат, состоящий из живых лиофилизированных бактерий B. infantis v. liberorum, L. acidophilus и Enterococcus faecium, устойчивых к антибиотикам и химиотерапевтическим средствам. Входящие в состав Линекса живые бифидобактерии, лактобациллы и нетоксигенный кисломолочный стрептококк группы D (выделенные из кишечника здорового человека) поддерживают и регулируют физиологическое равновесие кишечной микрофлоры во всех отделах кишечника. Выпускается в капсулах. В 1 капсуле содержится 1,2 x 107 живых кисломолочных бактерий (бифидо- и лактофлора). При его приеме создаются неблагоприятные условия для развития патогенной и условно-патогенной кишечной микрофлоры за счет продукции кисломолочной флорой уксусной, молочной и пропионовой кислот, что снижает рН кишечного содержимого. Прием препарата: взрослым по 2 капсулы 3 раза в день, детям — по 1 капсуле 3 раза в день. Хотя бактерии Линекса обладают кислотоустойчивостью, следует помнить, что при рН менее 3,5 они могут потерять свою жизнеспособность — соответственно препарат потеряет свои свойства. Поэтому принимать его рекомендуется после еды. Курс лечения зависит от степени выраженности дисбактериоза; в любом случае заместительная терапия должна быть продолжительной. Штаммы микроорганизмов, входящих в состав Линекса, являются специально выведенными, антибиотикоустойчивыми. Именно поэтому препарат можно назначать даже на фоне антибиотикотерапии. Как правило, микроорганизмы, входящие в состав пробиотиков, выполняют функцию временного заполнения экониши микрофлоры, которую со временем занимают колонии штаммов, изначально населяющих слизистую оболочку кишечника. В зависимости от степени дисбактериоза это замещение происходит в различные временные промежутки. Именно поэтому заместительная терапия пробиотиками должна носить достаточно длительный интермиттирующий характер.
Для усиления действия пробиотиков рекомендуется дополнительно назначать средства, обладающие противовоспалительными и иммуномодулирующими свойствами: Ф (Иммунал, Echinacea with Golden Seal), комплексные иммуномодулирующие препараты и витаминно-минеральные комплексы.
Оптимизация диагностики, индивидуализация лечения и проведение профилактики дисбактериоза кишечника позволят повысить эффективность терапии и обеспечат устойчивый бактериологический фон кишечника человека, что будет способствовать поддержанию хорошего качества жизни.
П. Л. Щербаков, доктор медицинских наук, профессор
НЦЗД РАМН, Москва