Как выглядят макрофаги под микроскопом
Макрофаги
Что такое клетки макрофаги и откуда они берутся?
Клетки макрофаги в самом деле большие: хотя их размер составляет всего 15-80 мкм, и человеческому глазу они не видны, однако они гораздо больше их предшественников: максимальный размер моноцита составляет всего 20 мкм. У них неправильная, «плавающая», меняющаяся форма, а их мембрана может образовывать ложноножки. Внутри макрофага находится ядро, а еще в нем обнаруживаются «осколки» эритроцитов и других клеток, жировые капельки, фрагменты бактерий и прочий «мусор». Как все это туда попадает? Очень просто, ведь макрофаги – это клетки, которые осуществляют процесс фагоцитоза.
Функции макрофагов:
При попадании в тело чужеродного объекта, будь то микроб или инородное тело, иммунная система сразу «спускает на него собак»: его атакуют фагоциты. Эти клетки, среди которых и макрофаги, распознают, улавливают и пожирают чужаков, угрожающих благополучию внутренней среды организма.
Кроме того, макрофаги уничтожают погибшие клетки, которые завершили свое существование процессом апоптоза (запрограммированная, естественная, нормальная гибель клеток). Также функции макрофагов заключаются в обеспечении противоопухолевого иммунитета: зафиксировав появление в организме атипичных, раковых клеток, макрофаги нападают на них и поедают.
Виды макрофагов:
Макрофаги – тканевые фагоциты, и в разных типах тканей нередко 
1. Альвеолярные макрофаги – находятся в стенках альвеол легких, очищают вдыхаемый воздух от различных загрязняющих и вредоносных частиц.
2. Купферовские клетки – в печени. Их назначение в основном заключается в уничтожении старых клеток крови.
4. Селезеночные макрофаги – располагаются в синусоидных сосудах этого органа. Как и у клеток Купфера, их задача заключается в том, чтобы вылавливать из крови и уничтожать отжившие клетки крови. Недаром селезенка называется кладбищем погибших эритроцитов!
5. Дендритные клетки – макрофаги, находящиеся под слизистыми оболочками и в коже, то есть фактически на границе с внешней средой.
6. Перитонеальные макрофаги – фагоциты, «живущие» в брюшине.
7. Где находятся макрофаги лимфатических узлов, понятно по названию. Это благодаря им лимфоузлы известны в качестве фильтров, очищающих лимфу.
Макрофаги и иммунная система:
Клетки макрофаги не просто бездумно уничтожают вредоносные объекты: расщепляя их на фрагменты, они осуществляют процесс презентации их антигенов. Антигены – это молекулы вредоносных частиц, которые говорят об их генетической чужеродности и вызывают соответствующую защитную реакцию со стороны иммунитета. Сами по себе они не представляют угрозы заражения или иного негативного воздействия, но это – метка чужака, поэтому организм реагирует на их присутствие защитной реакцией, как на полноценных агрессоров.
К сожалению, иногда личного опыта наших макрофагов или других фагоцитов недостаточно для того, чтобы иммунная система работала должным образом и правильно реагировала на вредоносные объекты. Чтобы повысить ее эффективность и заодно улучшить состояние здоровья в целом, рекомендуется принимать препарат Трансфер Фактор. Он содержит цитокины, несущие в себе данные о всевозможных возбудителях заболеваний, токсинах и прочих вредоносных агентах. Препарат обучает иммунитет полноценной работе, что немедленно и благоприятным образом отражается на течении имеющихся заболеваний, состоянии обмена веществ и функции органов. Средство можно использовать в лечебных и профилактических целях.
МАКРОФАГИ
МАКРОФАГИ (греч, makros большой + phagos пожирающий) — клетки соединительной ткани, обладающие активной подвижностью, адгезивностью и выраженной способностью к фагоцитозу. Макрофаги открыты И. И. Мечниковым; он впервые установил их роль в защитных и других реакциях организма и предложил термин «макрофаги», подчеркивающий отличия этих клеток от клеток меньшего размера — «микрофагов» (т. е. сегментоядерных лейкоцитов, нейтрофилов), фагоцитирующих лишь мелкие чужеродные частицы, напр. микробы. Макрофаги описывали под разными названиями: клазматоциты Ранвье, рагиокринные клетки, адвентициальные клетки, блуждающие клетки в покое, пирроловые клетки, полибласты, амебоидные, металлофильные клетки, макрофагоциты, гистиоциты. Большинство этих терминов имеет лишь исторический интерес.
М., как и все клетки соединительной ткани, имеют мезенхимное происхождение, а в постнатальном онтогенезе дифференцируются из стволовой кроветворной клетки (см. Кроветворение), проходя в костном мозге последовательно стадии монобласта, промоноцита и моноцита. Последние циркулируют в крови, и, выселяясь в ткани, превращаются в М. Различают М. свободные (мигрирующие) и фиксированные в тканях. М. также подразделяют на гематогенные, образующиеся из только что выселившихся из крови моноцитов, и гистиогенные, которые ранее присутствовали в тканях. В зависимости от локализации различают М. рыхлой соединительной ткани — гистиоциты (см.), печени — звездчатые ретикулоэндотелиоциты (купферовы клетки), легкого — альвеолярные М., серозных полостей — перитонеальные и плевральные М., М. костного мозга и лимфоидных органов, глиальные макрофаги ц. н. с. (микроглии). Из М. происходят, по-видимому, и остеокласты.
М., являясь последней стадией дифференцировки одноядерных фагоцитов, не делятся митозом. Исключение, возможно, составляют М. в очагах хрон, воспаления. На основе общего происхождения из стволовой кроветворной клетки, строения и функции М. и их клетки-предшественники (моноциты и др.), согласно классификации, опубликованной в Бюллетене ВОЗ (1973), включены в систему мононуклеарных фагоцитов. В отличие от этого ретикулоэндотелиальная система (см.) объединяет клетки, имеющие различное происхождение и обладающие способностью к фагоцитозу: ретикулярные клетки, эндотелиальные клетки (в частности синусоидные капилляры кроветворных органов) и другие элементы.
Строение М. отличается разнообразием, зависящим от фагоцитарной активности, свойств поглощенного материала и пр. (рис. 1). В отличие от своих предшественников моноцитов (см. Лейкоциты) М. имеют большие размеры (20—100 мкм), содержат много плотных цитоплазматических гранул и митохондрий; в слабобазофильной (иногда оксифильной) цитоплазме нередко видны остатки фагоцитированного материала. Ядро сферической, бобовидной или неправильной формы. При наблюдении в фазовом контрастном микроскопе в М. выявляется характерная ундулирующая клеточная мембрана, совершающая волнообразные движения. При электронной микроскопии в М. виден хорошо развитый пластинчатый комплекс (см. Гольджи комплекс), обычно небольшое количество гранулярного эндоплазматического ретикулума. Отражением фагоцитарной активности являются плотные цитоплазматические гранулы — лизосомы (см.), фагосомы, мультивезикулярные остаточные тельца — так наз. миелиновые фигуры (рис. 2). Наблюдаются также микротрубочки и пучки микрофиламент.
Функц, значение М. определяется их высокой способностью к поглощению и переработке плотных частиц — фагоцитоз (см.) и растворимых веществ — Пиноцитоз (см.).
Значение макрофагов в иммунитете
М. являются своеобразным накопителем поступающих в организм антигенов (см.), которые находятся в нем в виде детерминант (участков молекулы антигена, определяющих его специфичность), состоящих не менее чем из 5 пептидов. Антигены подвергают особой переработке: взаимодействуя с рецепторами мембраны М. антигены вызывают активацию их лизосомальных ферментов и увеличение синтеза ДНК.
М. играют весьма существенную роль в индукции антителообразования, для к-рой необходимы все три типа клеток (макрофаги, Т- и В-лимфоциты). Антиген, связанный с различными фракциями М. (мембраны, лизосомы), является значительно более иммуногенным, чем нативный антиген. После обработки в М. антигены поступают к Т- и B-лимфоцитам (см. Иммунокомпетентные клетки). М., содержащие антиген, вначале реагируют с Т-клетками, и только после этого «включаются в работу» В-клетки. Взаимодействие М. с Т-клетками регулируется Н-антигенами или продуктом гена, связанного с системой генов гистосовместимости (см. Иммунитет трансплантационный).
Макрофаги, Т- и В-лимфоциты взаимодействуют друг с другом при помощи разнообразных растворимых факторов, выделяемых этими клетками после антигенной стимуляции. Высказано предположение, что большинство растворимых факторов выделяется Т-лимфоцитами. Хим. природа этих факторов не изучена. Передача иммунол, информации от М. к лимфоциту происходит при непосредственном контакте этих клеток. Механизм этой передачи заключается в «прилипании» М. к лимфоциту, что сопровождается выбуханием цитоплазмы М., к-рая затем сливается с выростом цитоплазмы лимфоцита. М. синтезируют большое количество неспецифических факторов иммунитета: трансферрин, комплемент, лизоцим, интерферон, пирогены и др., являющиеся антибактериальными факторами.
М. играют большую роль в антимикробном и антивирусном клеточном иммунитете, чему способствует и относительно большая продолжительность жизни этих клеток (примерно от одного до нескольких месяцев), а также в развитии иммунного ответа организма. Они осуществляют важнейшую функцию по освобождению организма от чужеродных антигенов. Переваривание микробов или немикробных агентов, патогенных грибков, простейших, продуктов собственных измененных клеток и тканей осуществляется при помощи лизосомальных ферментов М.
Как показывают многочисленные исследования, идея И. И. Мечникова о значении фагоцитарных клеток в иммунитете (см.) справедлива в отношении не только бактерий, но и вирусов. М., особенно иммунизированных животных, принимают активное участие в разрушении вирионов (см. Вирусы), несмотря на то что вирусы более устойчивы к действию ферментов и процесс их разрушения идет менее энергично, чем процесс разрушения бактерий. М. выполняют защитную функцию на различных этапах инф. процесса: они являются барьером на месте входных ворот инфекции и на стадии виремии, когда ограничению распространения вируса препятствуют М. печени, селезенки и лимф, узлов. С помощью М. ускоряется процесс выведения вируса из организма, точнее, комплекса антиген— антитело (см. Антиген—антитело реакция). М., полученные от неиммунизированных и иммунизированных животных, активно фагоцитируют вирусы гриппа, осповакцины, миксомы, эктромелии. Из иммунных М. вирус гриппа мог быть выделен лишь в течение нескольких часов, в то время как из неиммунных М. он изолировался в течение нескольких суток.
Блокирование в эксперименте М. антимакрофагальной сывороткой, кремнием, каррагинаном (высокомолекулярная полигалактоза) приводит к отягощению течения ряда бактериальных и вирусных инфекций. Однако при некоторых вирусных заболеваниях М. оказались не только неспособными предотвратить инфекцию, но, более того, поддерживали репродукцию вирусов (напр., вирусов лимфоцитарного хориоменингита), которые длительно сохранялись в организме, способствуя развитию аутоиммунных заболеваний.
Проведены исследования, показавшие участие М. в цитотоксическом действии сенсибилизированных лимфоцитов на клетки-мишени. В эксперименте показано, что удаление м. из популяции иммунных лимфоцитов вызывало значительное ослабление цитотоксического действия лейкоцитов на клетки некоторых опухолей и что прогноз заболевания тем благоприятнее, чем больше активных М. содержится в регионарных к опухоли лимф, узлах. Изучение реакций иммунной системы реципиента при трансплантации органов и тканей показало, что М. участвуют в отторжении трансплантата и в элиминации чужеродных клеток из организма (см. Трансплантация).
Библиография: Бернет Ф. М. Клеточная иммунология, пер. с англ., М., 1971; Ван Фюрт Р. и др. Система мононуклеарных фагоцитов, новая классификация макрофагов, моноцитов и их клеток-предшественников, Бюлл. ВОЗ, т. 46, № 6, с. 814, 1973, библиогр.; Здродовский П. Ф. Проблемы инфекции, иммунитета и аллергии, М., 1969, библиогр.; Косяков П. Н. и Ровнова 3. И. Противовирусный иммунитет, М., 1972; Петров Р. В. Иммунология и иммуногенетика, М., 1976, библиогр.; Учитель И. Я. Макрофаги в иммунитете, М., 1978; Аllisоn А. С. Interactions of antibodies complement components and various cell types in immunity against viruses and pyogenic bacteria, Transplant. Rev., v. 19, p. 3, 1974, bibliogr.; Carr I. The macrophage, L.— N.Y., 1973; Gordon S. a. Сohn Z. The macrophage, Int. Rev. Cytol., v. 36, p. 171, 1973, bibliogr.; Immunobiology of the macrophage, ed. by D. S. Nelson, N. Y., 1976; Mononuclear phagocytes in immunity, ed. by R. van Furth, Oxford, 1975; Wahl S. M. a. o. The role of macrophages in the production of lymphokines by T and B lymphocytes, J. Immunol., v. 114, p. 1296, 1975.
H. Г. Хрущов; М. С. Бердинских (иммунол.).
Иммунные клетки помогают сердцу биться
Клетки макрофаги помогают волокнам проводящей системы сердца держать ритм.
Сердце сокращается благодаря системе особых мышечных волокон, которые не похожи на те, что составляют основную массу сердца, и которые сами генерируют сократительный импульс, распространяя его на всю сердечную мышцу.
Эти волокна образуют несколько разных отделов, и начинается все с так называемого синоатриального узла в правом предсердии. Синоатриальный узел называют водителем ритма первого порядка, из него импульс переходит в предсердно-желудочковый (атриовентрикулярный) узел, который находится на границе между предсердиями и между правым предсердием и правым желудочком. Затем сократительный сигнал распространяется по другим волокнам, так что все отделы сердца работают ритмично и согласованно.
Но в сердце есть не только обычные мышечные волокна и атипичные, генерирующие ритм – в нем есть и другие клетки, среди которых довольно много иммунных макрофагов. Задача макрофагов – искать и уничтожать бактерии, убирать клеточный мусор, помогать ранам заживать и т. д. Но в сердце у них есть еще одна, совершенно неожиданная функция. Исследователи из Гарвардской медицинской школы решили выяснить, зачем сердцу так много макрофагов, и убрали их из сердечной мышцы мыши – и тут оказалось, что «обезмакрофаженное» сердце плохо бьется, что сократительный импульс часто просто пропадает на границе между правым предсердием и правым желудочком. Дальнейшие эксперименты показали, что в этой зоне макрофагов особенно много, что у мышей, что у людей.
Когда иммунные клетки попробовали вырастить в одной культуре вместе с мышечными, то оказалось, что макрофаги тесно соединяются с мышечными клетками; более того, электрохимические параметры клеточной мембраны макрофагов оказываются согласованы с электрохимическими параметрами их мышечных партнеров – то есть клетки синхронизируют свои электрические особенности.
Чтобы узнать, как иммунные и мышечные клетки взаимодействуют в сердце, авторы работы модифицировали макрофаги так, чтобы заряд на их мембране можно было регулировать световым импульсом: когда клетка получала порцию света по оптоволокну, она делалась более положительно заряженной. Такой «положительный» макрофаг, в свою очередь, повышал возбудимость соседних мышечных клеток – они с большей готовностью принимали и проводили электрический импульс.
Когда мышиное сердце заставляли биться быстрее обычного, то некоторые импульсы, рожденные в предсердном водителе ритма, не доходили до желудочков, теряясь в районе атриовентрикулярного узла. Но если модифицированные макрофаги, которые сидели тут же, в этом же узле, стимулировали светом, то атриовентрикулярный узел проводящих волокон начинал работать без перебоев. То есть иммунные клетки, становясь положительно заряженными, помогали работать клеткам сердца, которые под влиянием макрофагов лучше чувствовали приходящие импульсы и передавали их дальше по сердечной мышце. Подробно результаты экспериментов опубликованы в статье в Cell.
Очевидно, что макрофаги помогают работать сердцу и в обычной ситуации, без каких-то модификаций. О том, что сердце, лишенное их, начинает плохо работать, мы уже говорили; то же самое происходило, когда у мышей отключали ген белка, соединяющего макрофаги с мышечными клетками – тесный контакт между ними исчезал, и иммунные клетки уже не могли влиять на своих мышечных партнеров. Возможно, что некоторые проблемы, связанные с аномальным сердечным ритмом, возникают из-за того, что макрофаги и проводящие волокна сердца утрачивают контакт друг с другом. Если так, то, возможно, в ближайшем будущем мы сможем лечить сердце, действуя через иммунную систему.
Функции макрофагов в различных условиях микроокружения опухоли
Связанные с опухолью макрофаги, как известно, стимулируют ключевые этапы прогрессирования опухоли. В этом обзоре рассказывается о многочисленных экспериментальных и клинических исследованиях, проведенных с целью изучения функций, регуляции и клинической значимости опухолевых макрофагов. В отношении клинической значимости наиболее интересны три участка инвазии раковых клеток: опухолевые гнезда, пограничная зона между стромой и опухолевыми клетками, а также области, близкие к сосудистой сети опухоли или удаленные от нее. Более полное понимание разнообразия опухолевых макрофагов может привести к разработке избирательных методов лечения, основанных на восстановлении противораковых функций этих клеток.
Вступление
Опухолевые макрофаги (ОМ) изобилуют в большинстве типов злокачественных новообразований, способствуют опухолевому ангиогенезу, выходу раковых клеток из опухоли в кровоток, способствуют их выживанию и постоянному росту в метастатических колониях, подавлению противоопухолевых иммунных механизмов. В то же время ОМ могут подавлять, дополнять или опосредовать противоопухолевые эффекты цитотоксических агентов, лучевой терапии, антиангиогенных препаратов и ингибиторов контрольных точек.
Происхождение этих клеток в настоящее время является предметом обсуждения. Недавние исследования показали, что макрофаги во многих тканях происходят не из циркулирующих моноцитов, как первоначально предполагалось, а из эмбриональных макрофагов (особенно из макрофагов желточного мешка), которые закладываются в тканях во время развития. Эти предшественники остаются в тканях взрослого организма и размножаются, таким образом, сохраняясь независимо от гемопоэтической системы взрослого человека. В некоторых органах, например, в кишечнике, основные популяции макрофагов развиваются путем рекрутирования моноцитов. Выборочное истощение каждого из этих двух подтипов ОМ показало, что только эмбриональные макрофаги поддерживают опухолевый рост.
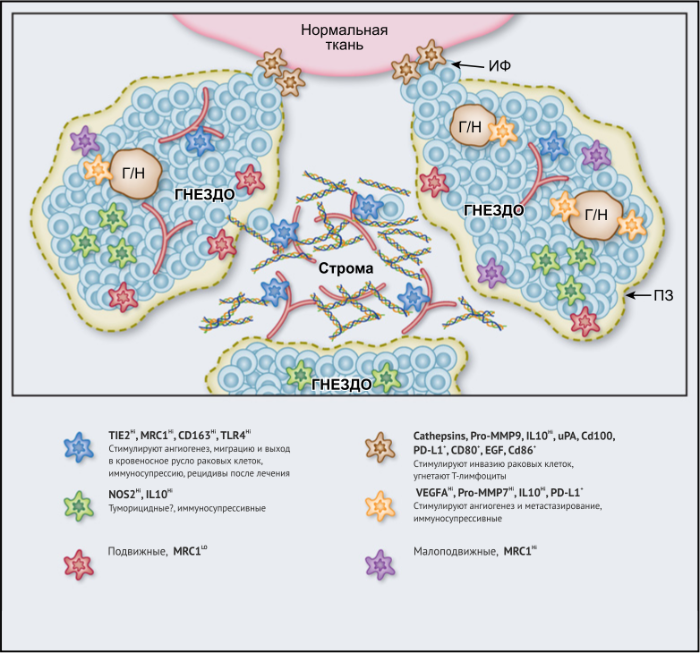
ОМ могут находиться в различных состояниях активации. Обычно они отклоняются от «классически» активированного, агрессивного по отношению к опухоли фенотипа (иногда называемого M1) в сторону «альтернативно» активированного опухолевого промотора (M2). Однако как и макрофаги во многих других тканях, ОM обладают замечательной функциональной пластичностью и часто экспрессируют маркеры, характерные для обоих состояний активации, что делает такой полярный подход к их классификации неточным. Предполагается, что функции ОМ могут, по крайней мере частично, регулироваться их расположением в опухоли; что они проявляют разные функции по меньшей мере в трех областях инвазии раковых клеток: области высокой плотности раковых клеток (так называемом «опухолевом гнезде»); периваскулярной (ПВ) нише; и плохо васкуляризованных гипоксических/некротических областях опухоли (Рис.1 и 2).
Области инвазии
Существует по крайней мере три основных локализации, в которых прогрессия опухоли была ассоциирована с повышенной инвазией клеток.
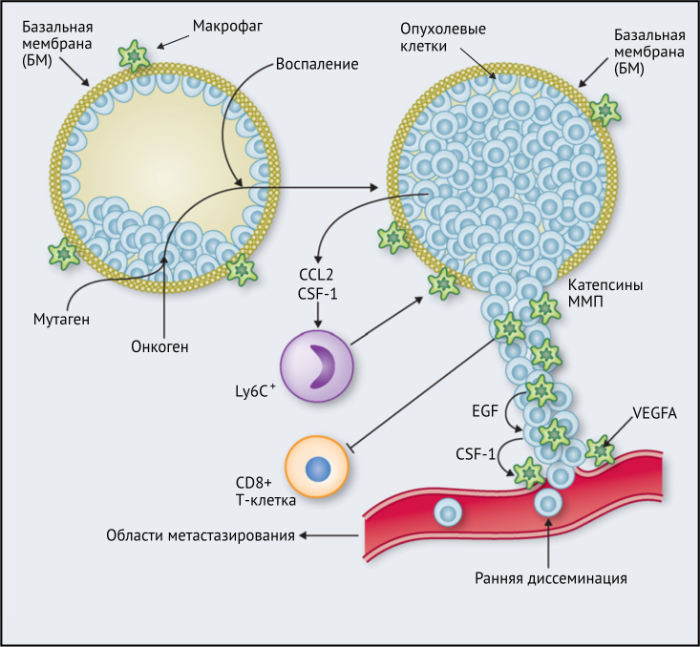
Результаты исследований, проведенных на мышах, показывают, что макрофаги способствуют развитию злокачественных опухолей различными способами: реконструируют внеклеточный матрикс, опосредуют разрушение базальной мембраны, увеличивают подвижность раковых клеток, и их способность к миграции, способствуют прогрессированию преинвазивных поражений, выделяют фактор роста эндотелия сосудов A (VEGF-A). Макрофаги вокруг преинвазивных поражений молочных желез у мышей высвобождают CXCR2-связывающие хемокины CXCL1 и CXCL5, которые способствуют миграции и инвазии соседних предростопластических (предраковых) эпителиальных клеток. В то же время подавление активности макрофагов вызывало замедление развития инвазии опухолевых клеток и развития опухоли в целом.
Недавнее исследование на модели рака легких Kras G12D показало, что нарушение регуляции онкогенов, таких как Myc, в раковых клетках вызывает трансформацию медленно прогрессирующей аденомы легкого в агрессивную аденокарциному. Это связано с тем, что изменения в Myc стимулировали увеличение экспрессии CCL9 и IL-23 эпителиальными клетками легких. CCL9 затем стимулировал накопление VEGFA + макрофагов и, следовательно, ангиогенез опухоли, а также PD-L1-зависимое вытеснение T- и B-клеток. Кроме того, IL-23 стимулировал гибель Т- и В-клеток и цитотоксических NK-клеток (Рис.1).
Следует отметить, что антитела против CD68 продолжают широко использоваться в качестве иммунных меток ОМ в опухолях (Таблица 1). Однако как и многие другие антитела, маркирующие отдельные типы клеток, человеческие анти-CD68 иногда маркируют клетки, отличные от ОM. Например, методом качественного анализа с помощью иммуноокрашивания удалось установить, что некоторые клетки CD68 + в опухолях молочной железы человека не экспрессируют рецептор к КСФ-1 (КСФ-1Р), CD45 или другие маркеры эпителиальных клеток, эндотелиальных клеток или клеток стенок сосудов (то есть гладкомышечных клеток, перицитов или фибробластов). Остается неизвестной как принадлежность этих клеток, так и то, маркируются ли они антителами к CD68 иного происхождения.
ОМ в ИФ опухоли поджелудочной железы RIP1-Tag2 мыши усиливают инвазивный потенциал раковых клеток посредством экспрессии катепсинов B и S, двух ферментов, регулируемых IL-4, высвобождаемым раковыми клетками и инфильтрирующими опухоль Т-клетками. Кроме того, было показано, что CD4 + Т-клетки в опухолях MMTV-PyMT увеличивают инвазивность раковых клеток благодаря IL-4, что затем стимулирует ОM экспрессировать эпидермальный фактора роста (EGF).
Эти экспериментальные данные хорошо согласуются с данными исследований, согласно которым ОM в ИФ опухолей желудка человека выделяют MMP9 — фермент, разрушающий матрикс, — и рецептор сериновых протеаз, урокиназный активатор плазминогена (УАП, урокиназа). Интересно, что ОМ вдоль ИФ первичной карциномы толстой кишки экспрессируют CD80 и CD86 (костимуляторные сигналы, необходимые для активации Т-клеток), что указывает на то, что они могут иметь потенциал для стимулирования противоопухолевого иммунитета при этом типе рака. Это может объяснить наблюдение, что повышенное количество CD68 + ОM в ИФ колоректальных опухолей человека коррелируют с более высокой выживаемостью без рецидива (RFS) (Таблица 1). Тем не менее, в ИФ опухолей могут присутствовать различные ОM-подмножества, причем некоторые из них являются иммуносупрессивными. Например, ОM в ИФ гепатоцеллюлярных карцином (ГЦК) экспрессируют более высокое количество лиганда иммуносупрессивной контрольной точки PD-L1, чем ОМ в других опухолевых гнездах, и связаны с плохой выживаемостью. Кроме того, было показано, что семафорин 4D (SEMA4D, CD100) — цитокин, экспрессия которого особенно выражена в ИФ опухоли толстой кишки Colon26, стимулирует ОM, которые экспрессируют иммуносупрессивный цитокин IL-10 в ИФ, и таким образом подавляют активированные CD8 + Т-клетки. Блокада антител SEMA4D подавляла ОМ в ИФ и повышала эффективность лечения ингибиторами контрольных анти-PD-1 и анти-CTLA4 (Рис.2).
Опухолевые гнезда
Возможные функции ОМ в непосредственной близости от раковых клеток в опухолевых «гнездах», по-видимому, варьируются в зависимости от типа опухоли. Например, ОM, экспрессирующие NOS2 — фермент, связанный с их цитотоксическим потенциалом, — обнаруживаются в тесном контакте с раковыми клетками в некоторых опухолях предстательной железы, а большое количество ОM в опухолевых гнездах коррелирует с улучшенным прогнозом при раке эндометрия, а также снижением количества рецидивов рака желудка (Таблица 1). Повышенное количество ОM коррелирует с уменьшенной общей выживаемостью и RFS при злокачественных меланомах, а также опухолях молочной железы и пищевода (Таблица 1). ОМ в гнездах ГЦК человека экспрессируют IL-10 и рекрутируют иммуносупрессивные клетки FoxP3 + Treg, хотя нет данных, что эти Treg влияют на исход заболевания (Рис. 2).
Интересно, что ОМ экспрессируют сигнальный регуляторный белок альфа (SIRP-α) на своей поверхности, который связывается с трансмембранным белком CD47 на злокачественных клетках. Когда это происходит, подавляется способность ОM обнаруживать и фагоцитировать опухолевые клетки. Различные исследования показали, что блокирование CD47 прерывает этот сигнал «не ешь меня» и вызывает разрушение опухолей при посредстве ОM у мышей, а высокая экспрессия CD47 обуславливает плохой прогноз рака мочевого пузыря, острого миелоидного лейкоза, неходжкинских лимфом и рака молочной железы. Так опухолевые клетки уклоняются от наблюдения ОМ.
Строма
В области стромы большинства солидных опухолей опухолевых клеток обычно мало либо нет вовсе. Она состоит из сложной сети макромолекул, формирующих внеклеточный матрикс(ВКМ), к которым относятся коллагеновые фибриллы, ламинин, фибронектин, тенасцин C и гиалуроновая кислоту (ГК). В нем часто находятся популяции различных клеток, включая фибробласты, эндотелиальные клетки, перициты, лимфоциты и миелоидные клетки. Ряд исследований показал, что компоненты ВКМ (и/или продукты его протеолиза), такие как фибронектин, ламинин-10, версикан (хондроитинсульфатсодержащий протеогликан) и фрагменты ГК, регулируют фенотип макрофагов. Пинто и его коллеги в исследованиях in vitro показали, что бесклеточный ВКМ, выделенный из колоректальных опухолей, стимулирует макрофаги экспрессировать IL-10, TGF-β и снижает экспрессию рецепторов хемокинов C-C 7 (CCR7), TNF-α и IL-6. Кроме того, повышенная экспрессия стромальными ОМ лигандов хемокинов C-C 18 (CCL18) связана с повышенным метастазированием и снижением выживаемости у пациентов при раке молочной железы. Это согласуется с рядом исследований, свидетельствующих о корреляции между большим количеством стромальных ОМ и низкой общей выживаемостью и RFS при опухолях молочной железы, пищевода, желудка, поджелудочной железы, орофациальных, кожных (Таблица 1). Существует зависимость от типа опухоли, поскольку такой корреляции при раке эндометрия, шейки матки и легких не выявлено, а при раке мочевого пузыря прослеживается уменьшение метастазирования в лимфатических узлах и улучшение выживаемости (Таблица 1).
Помимо описанных выше химических компонентов стромы опухоли, функции ОМ также регулируют ее биофизические свойства. Архитектоника и плотность ВКМ регулирует экспрессию различных провоспалительных генов макрофагами in vitro путем активации сигнальных путей TLR4 в этих клетках. Высокие уровни 22 общих составляющих матрикса («меток матрикса») положительно коррелируют как с плотностью опухоли, так и с инфильтрацией ОМ при метастазах рака яичников, хотя еще предстоит выяснить, есть ли причинно-следственная связь между инфильтрацией и структурой опухоли. Также следует отметить, что разные области стромы при данной опухоли могут различаться по своим химическим и биофизическим свойствам и влиять на ОМ по-разному (Рис. 2).
Периваскулярная ниша
Подмножество ОМ лежит близко или на поверхности кровеносных сосудов в опухолях мышей и человека. Эти клетки часто экспрессируют большое количество маркеров, связанных с M2: TIE2 (основной рецептор ангиопоэтина), MRC1 и CD163, — и играют ключевую роль в стимулировании ангиогенеза опухоли, метастазирования и рецидива после терапии первой линии. Из-за их относительно высокой экспрессии TIE2 эти клетки первоначально назывались «TIE2-экспрессирующие моноциты/макрофаги (TEM)». Частота TEM также положительно коррелирует с плотностью микрососудов (MVD) у некоторых типов опухолей человека (Табл. 1).
Генетическая делеция периваскулярных (ПВ) TIE2 + ОМ или фармакологическая блокада основного лиганда TIE2 — ангиопоэтина 2 (AGPT2), — продемонстрировали важную роль этого подмножества ОM в ангиогенезе опухоли и ее росте у различных мышиных моделей рака. Стимуляция экспрессии генов TEM, выделенных из опухолей мыши, привела к более высокой экспрессии ряда генов, способствующих развитию опухолей, включая Mmp9, Vegfa, Cxcl12, Tlr4 и Nrp1, чем TIE2- ОM из тех же опухолей.
ПВ TIE2 + ОM также участвовали в рецидиве первичных опухолей мыши после различных форм лечения. Они учащают рецидивы глиомы после местного облучения, а также при опухолях легких и молочной железы после химиотерапии. В такие моменты они экспрессируют большое количество CXCR4 и рекрутируются с помощью активированного CXCL12 в ПВ нише. Это подмножество ОМ затем стимулирует реваскуляризацию и рост опухоли посредством высвобождения VEGF-A. Позднее исследование подтвердило, что экспрессия TIE2 в ОМ необходима для стимуляции васкуляризации после химиотерапии у мышей. Кроме того, недавно рекрутированные моноциты также мигрируют вокруг опухолей, не подвергавшихся терапии, зависимым от CXCR4 образом. Меченые моноциты проникали в ПВ зону опухоли PyMT, где они затем подвергались воздействию TGFβ, выделяемого раковыми клетками, что стимулировало эти моноциты повышать свою экспрессию CXCR4 и мигрировать к CXCL12-экспрессирующим фибробластам вокруг опухолевых кровеносных сосудов в богатых коллагеном стромальных областях. Как только они примыкают к сосудам, моноциты дифференцируются в «метастаз-ассистирующие» ПВ ОM, участвующие в TMEM.
Наконец, в метастатических областях, таких, как легкие, подмножество макрофагов CCR2 + Ly6C + способствует выходу раковых клеток в кровеносное русло и образованию из них метастазов. Эти «метастаз-ассоциированные макрофаги» (MAM) были использованы в мышиных моделях опухолей, чтобы напрямую связать молекулу адгезии сосудистых клеток-1 (VCAM-1) с раковыми клетками через их α4-интегрины. Этот процесс впоследствии увеличивает выживаемость раковых клеток в таких метастатических областях. Кроме того, связывание CCL2 с CCR2 на MAM стимулирует высвобождение ими CCL3, который связывается с CCR1 на раковых клетках и облегчает их удержание в легких. Эти MAM также способствуют постоянному росту метастатических повреждений с помощью сигналов VEGFR1 и CSF-1R.
Гипоксические/некротические области
Гипоксия является отличительной чертой солидных опухолей и связана с увеличением инвазии и метастазов, сопротивлением терапии и плохим клиническим исходом. Гипоксические области обычно имеют парциальное давление кислорода (рО2) ниже 10 мм рт. ст. Они расположены более чем в 150 мкм от опухолевых кровеносных сосудов. Они образуются в опухолях, когда потребность клеток в кислороде опережает их снабжение плохо организованными опухолевыми сосудами. Эти области были идентифицированы в опухолевых срезах с использованием маркеров гипоксических клеток, например, пимонидазола, или иммуноблока для индуцируемой гипоксией альфа-субъединицы транскрипционных факторов HIF 1 и 2. Большое количество гипоксических ОМ ассоциируется с повышенным уровнем ангиогенеза опухолей, метастазами, сниженной RFS и/или снижением общей выживаемости при раке молочной железы, эндометрия и шейки матки (Таблица 1).
ОM в таких областях регулируют HIF 1 и 2 и различные гены-мишени HIF, такие как VEGF-A, GLUT1 и MMP7. Хемокины, усиливающие гипоксию, рекрутируют в гипоксические области ОМ, в том числе хемокин C-X-C 12 (CXCL12), полипептид-активирующий эндотелий-клеточный моноцит II (EMAP-II), эндотелин 2, VEGF-A и SEMA3A. Гипоксические ОМ иммобилизируются в этих областях прямым ингибирующим действием гипоксии на их подвижность и снижением экспрессии их рецепторов опухолевых хемокинов CCR2, CCR5 и NRP1.
Гипоксические ОМ способствуют ангиогенезу опухоли, уклонению от иммунитета и метастазированию в различных экспериментальных моделях. Например, они регулируют экспрессию большого количества проангиогенных и иммуносупрессивных цитокинов в гипоксических зонах опухоли, а когда их проникновение в гипоксические области опухолей затруднено сигнальной блокадой SEMA3A/NRP1, опухолевый ангиогенез заметно снижается и противоопухолевый иммунитет восстанавливается. Гипоксические ОМ также способны подавлять активацию Т-клеток различными способами, влияя на IL-10 и на контрольные точки, например, через лиганд PD-L1. Макрофаги, кокультивированные с клетками ГЦК в гипоксических условиях, увеличивают экспрессию индоламин 2,3-диоксигеназы (IDO), которая подавляет пролиферацию местных цитотоксических Т-клеток и увеличивает популяцию клеток Treg.
Хотя воздействие гипоксии само по себе не может изменить фенотип ОМ в отношении стимуляции роста опухоли, некоторые исследования показали, что низкий уровень рН и лактат (которые накапливаются в слабо васкуляризированных, гипоксических областях из-за плохого сосудистого питания) совместно индуцируют проангиогенный фенотип ОМ, который, в свою очередь, восстанавливает перфузию крови. Действительно, молочная кислота может стимулировать экспрессию VEGF-A макрофагами. Как упоминалось ранее, этот цитокин является не только проангиогенным в опухолях, но также способен стимулировать выход в сосуды раковых клеток.
Опухолевая гипоксия также может модулировать функции ОМ опосредованно, стимулируя раковые клетки выделить белок группы 1 с высокой подвижностью (HMGB1), который, в свою очередь, стимулирует продукцию IL-10 ОM. Гипоксия также индуцирует метаболические изменения в ОМ, которые затем непосредственно влияют на функции соседних клеток. Например, гипоксия стимулирует экспрессию REDD1, ингибитора mTOR и ключевого модулятора метаболизма в ответ на доступность питательных веществ и потребность в энергии. Ингибирование mTOR в ОM сильно снижает их поглощение глюкозы и активность гликолиза, оставляя больше глюкозы для соседних эндотелиальных клеток. Это повышает способность раковых клеток проникать в сосудистое русло, соответственно, приводит к формированию отдаленных метастазов.
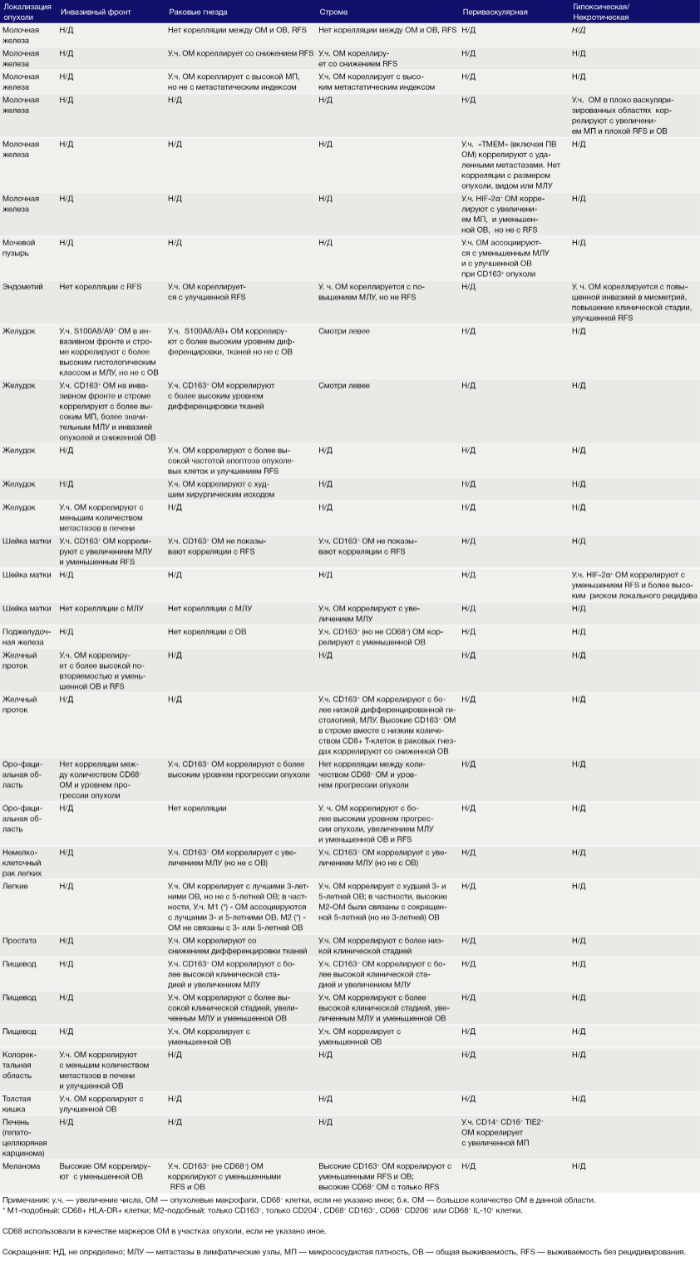
Таблица 1. Опухолевые макрофаги в различных злокачественных новообразованиях человека: корреляция с клинико-патологическими проявлениями
Заключение
Ряд экспериментальных исследований на мышах подтвердил способность различных опухолевых популяций дифференцированно регулировать фенотип ОМ. Важность этого подчеркивается клиническими отчетами, показывающими, что число или фенотип ОМ в определенных областях опухоли коррелируют с RFS и выживаемостью (Таблица 1).
Имеются данные о роли подмножеств ОM в определенных областях опухолей, ограничивающих ответ опухолей на лечение. Например, облучение, сосудистые разрушающие агенты и цитотоксические препараты индуцируют пролиферацию ПВ ОM, что способствует ангиогенезу опухоли и рецидиву после терапии. Гипоксические ОМ также были вовлечены в устойчивость опухолей к противоопухолевой терапии и способствуют рецидиву.
Демонстрация того, что ОМ стимулируют ряд механизмов опухолеобразования на мышиных моделях опухолей, побудила к развитию терапевтических подходов к истощению или перепрограммированию ОМ. На сегодняшний день общие ингибиторы ОМ, включая те, которые нацелены на CSF-1-CSF-1R и CCL-CCR2, в значительной степени не показали эффективности в клинических испытаниях в качестве монотерапии рака, хотя они могут оказаться эффективными в сочетании с другими терапевтическими агентами. Ингибитор CSF-1-R PLX3397 показал значительную эффективность при лечении теносиновиальной гигантоклеточной опухоли, лечение также выявило побочное действие, вызванное долгосрочным истощением всех макрофагов.
Таргетная терапия в отношении определенных ОM-подмножеств в опухолях может стать отличным методом в качестве противоопухолевой терапии посредством истощения или перепрограммирования тех ОМ, которые способствуют с помощью различных механизмов опухолевой прогрессии, при этом она должна оставлять или усиливать те подмножества ОМ, которые способствуют противоопухолевому иммунитету. Прогресс в нашем понимании того, как фенотип подмножеств ОМ в различных областях опухоли зависит от их онтогенеза, статуса активации и сложного комплекса местных взаимодействий поможет разработать такой терапевтический подход. Раскрытие сложного массива влияний на поведение ОM потребует многогранного подхода к исследованиям, однако это может привести к появлению новых возможностей в лечении опухолевых заболеваний, появлению новых таргетных противоопухолевых препаратов.
Источник: Yang M. et al. Diverse Functions of Macrophages in Different Tumor Microenvironments //Cancer research. – 2018. – Т. 78. – №. 19. – С. 5492-5503.