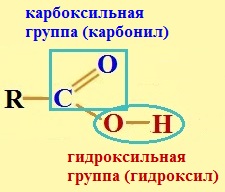
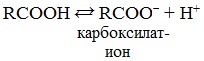Как выглядит формула карбоксильной группы
Как выглядит формула карбоксильной группы
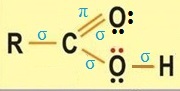
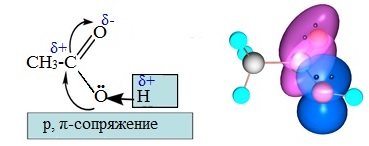
С атомом кислорода карбонильной группы атом углерода образует еще одну связь. Негибридизованные р-орбитали атома углерода и карбонильного атома кислорода перекрываются с образованием π-связи.
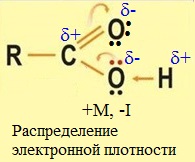
В карбонильной группе электронная плотность смещена к атому кислорода в силу его высокой электроотрицательности. Вследствие этого на карбонильном атоме углерода возникает частичный положительный заряд.
Атом углерода стремится компенсировать положительный заряд и притягивает к себе неподеленную пару электронов атома кислорода гидроксильной группы.
В свою очередь, атом кислорода оттягивает на себя электронную плотность по связи О-Н от атома водорода гидроксогруппы.
Вследствие этого связь между атомами кислорода и водорода в гидроксильной группе становится более полярной и атом водорода приобретает повышенную подвижность, что существенно упрощает его отрыв в виде протона (Н + ).
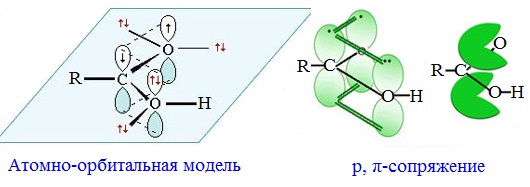
Карбоксильная группа представляет собой плоскую p,π-сопряженную систему за счет взаимодействия р-электронов атома кислорода гидроксильной группы с электронами π-связи карбонильной группы.
р-Орбиталь атома кислорода гидроксильной группы, содержащая неподеленную пару электронов, сопряжена с π-орбиталью карбонильной С=О- группы.
В результате взаимного влияния атомов в карбоксильной группе связь С=О более прочная, чем в карбонильной группе альдегидов, а связь О-Н менее прочная, чем в спиртах.
Кислотные свойства карбоновых кислот обусловлены смещением электронной плотности к карбонильному атому кислорода и вызванную этим сильную поляризацию связи О-Н (по сравнению со спиртами и фенолами), в результате чего облегчается отрыв атома водорода в виде протона.
Карбоновые кислоты в отличие от спиртов диссоциируют с образованием ионов водорода Н:
Для карбоновых кислот, в отличие от альдегидов, не характерны реакции присоединения по двойной связи >С=О, за счет уменьшения положительного заряда на карбонильном атоме углерода атомом кислорода гидроксогруппы.
Карбонильные соединения
Содержание:
Карбонильные соединения не образуют между собой водородных связей, поскольку в их молекулах нет атомов водорода с частичным положительным зарядом `delta+` на нём. Формальдегид – газ, остальные – жидкости или твёрдые вещества.
На странице -> решение задач по химии собраны решения задач и заданий с решёнными примерами по всем темам химии.
Карбонильные соединения
Карбонильные соединения – это органические вещества, молекулы которых содержат карбонильную группу
Строение карбонильныx соединений
Альдегиды и кетоны относятся к карбонильным соединениям. Карбонильные соединения — это производные углеводородов, которые содержат карбонильную группу C = O.
Альдегиды — это карбонильные соединения, в молекулах которых карбонильная группа связана с атомам водорода и углеводородным радикалом. Исключением является формальдегид, или муравьиный альдегид. В этом соединении карбонильная группа соедийена с двумя атомами водорода:
Молекулы всех альдегидов содержат функциональную группу
Общая формула альдегидов:
Модели молекул метаналя и этаналя представлены на рис 7.

Рис. 7. Модели молекул: а) метаналя 6) этаналя
В кетонах карбонильная группа связана с двумя одинаковыми или разными углеводородными радикалами. Простейший представитель кетонов — ацетон (рис. 8).

Рис. 8. а) структурная формула ацетона; б) модель молекулы ацетона
Общая формула кетонов:
Строение молекулы. Рассмотрим электронное строение формальдегида

Рис. 9
Изомерия и номенклатура. У альдегидов различают изомерию углеродного скелета и межклассовую изомерию с кетонами. Для кетонов характерна изомерия углеродного скелета и положения карбонильной группы.
Для альдегидов разветвленной цепью перед названием указывают положения заместителей в углеродной цепи. Например,
Названия кетонов производят от названии соответствующих алканов с добавлением суффикса —он:
Получение альдегидов и кетонов
В лаборатории альдегиды получают окислением первичных спиртов. В качестве окислителей применяют оксид меди (II), пероксид водорода, перманганат калия и другие вещества.
1. Окисление спиртов.
Проведем такой опыт. Накалим в пламени спиртовки спираль из медной проволоки и опустим ее в пробирку со спиртом. Мы заметим, что проволока, покрывающаяся при нагревании темным налетом оксида меди (II), в спирте вновь становится блестящей, одновременно обнаруживается запах альдегида:
В общем виде окисление спиртов можно показать так:
При окислении первичных спиртов образуются альдегиды. При окислении вторичных спиртов образуются кетоны.
Для простоты окислитель обозначают в виде атома кислорода. В промышленности основную массу формальдегида производят из метанола, пропуская его пары вместе с воздухом через реактор с раскаленной сеткой из меди или серебра:
2. Гидратация алкинов.
Гидратация алкинов-присоединение воды к алкинам (реакция Кучерова).
Этаналь получают в промышленности преимущественно гидратацией ацетилена в присутствии солей ртути в качестве катализатора (реакция Кучерова).
Кетоны получают:
а) при гидратации гомологов ацетилена:
б) при окислении пропилена:
3. Окисление алкенов. Ацетальдегид можно получить из этилена окислением кислородом в присутствии медных, железных и палладиевых катализаторов. Для этого смесь этилена с воздухом пропускают через раствор солей меди, железа и палладия. Упрощенно процесс можно показать так:
Этот способ более перспективен, чем гидратация алкинов, при котором используются токсичные ртутные катализаторы.
4. Кумольный способ получения ацетона
Альдегиды и кетоны относятся к карбонильным соединениям. Карбонильные соединения — это производные углеводородов, которые содержат карбонильную группу
Химические свойства, применение альдегидов и кетонов
Физические свойства. Альдегиды и кетоны — полярные вещества с избыточной электронной плотностью на атоме кислороде. Низшие члены ряда альдегидов и кетонов растворимы в воде. Их температуры кипения ниже, чем у соответствующих спиртов. Метаналь (формальдегид) — бесцветный ядовитый газ с резким запахом. Водный 35—40% раствор формальдегида называют формалином.
Остальные члены гомологического ряда альдегидов — жидкости, а высшие альдегиды — твердые вещества.
Ацетон — легколетучая жидкость.
Химические свойства.
1. Реакции восстановления. Альдегиды и кетоны способны присоединять водород по двойной связи; альдегиды образуют при этом первичные спирты, кетоны — вторичные:
Если, например, пары метаналя вместе с водородом пропускать над
нагретым никелевым катализатором, то происходит присоединение водорода. Формальдегид восстанавливается до метилового спирта.
Подобные уравнения реакций можно составить и для других альдегидов.
2. Реакции окисления.
Под влиянием карбонильного атома кислорода альдегиды окисляются по связи C—H в альдегидной группе. Если в чистую пробирку налить аммиачный раствор оксида серебра Ag2O, прибавить к нему раствор альдегида и смесь осторожно нагреть, то на стенках пробирки появится блестящий налет серебра. В этой окислительно-восстановительной реакции альдегид превращается в кислоту, а серебро выделяется в свободном виде:
Такая реакция называется реакцией “серебряного зеркала«, и она является качественной реакцией на альдегиды (рис. 10).

Рис. 10. Реакция «серебряного зеркала»
В качестве окислителя альдегидов может быть использован также гидроксид меди (II) Cu(OH)2. Если к голубому осадку гидроксида меди (II) прилить раствор альдегида (в щелочной среде) и смесь нагреть, то сначала появляется желтый осадок CuOH, который затем превращается в красный оксид меди (I) Cu2O. В данной реакции гидроксид меди (II) окисляет альдегид в соответствующую карбоновую кислоту, а сам восстанавливается до оксида меди (I).
Эта реакция также является характерной реакцией для альдегидов.
В отличие от альдегидов кетоны не окисляются оксидом серебра (I) и гидроксидом меди (II). Карбонильные соединения, особенно альдегиды, весьма реакционноспособные соединения.
3. Реакции присоединения. Химическая активность карбонильных соединений, их высокая реакционная способность определяется карбонильной группой. Альдегиды и кетоны способны вступать в реакции присоединения. Связь C=O полярна, на атоме углерода сосредоточен частичный положительный заряд. Такие реакции начинаются с взаимодействия атома углерода карбонильной группы со свободной электронной парой нуклефилъного реагента (Nu ). Затем образовавшийся анион присоединяет протон или другой катион:
При нуклеофильном присоединении синильной кислоты в присутствии следов щелочей к альдегидам и кетонам образуются оксинитрилы:
Альдегиды и кетоны вступают в реакцию нуклеофильного присоединения с гидросульфитом натрия:
Образующиеся при этом гидр ©сульфитные производные карбонильных соединений при нагревании с минеральными кислотами или содой разлагаются с образованием исходных карбонильных соединений:
Применение. Формальдегид применяется в производстве фенолформальдегидных смол, красителей, синтетического каучука и взрывчатых веществ. Его водный раствор формалин используется для бальзамирования различных органических веществ, органов и организмов, консервирования анатомических препаратов, для выделывания кожи и дезинфекции.
Ацетальдегид применяют в основном для получения уксусной кислоты, а также в некоторых органических синтезах.
Высшие альдегиды, содержащие молекулах от 7 до 16 атомов углерода, широко применяются в парфюмерии, так как обладают приятным запахом. Ацетон и другие кетоны являются хорошими растворителями лаков, красок и синтетических смол.
Альдегиды и кетоны способны присоединять водород по двойной связи; альдегиды образуют при этом первичные спирты, кетоны — вторичные. Под влиянием карбонильного атома кислорода альдегиды окисляются по связи C—H в альдегидной группе и превращаются в карбоновые кислоты. В отличие от
альдегидов кетоны не окисляются оксидом серебра (I) и гидроксидом меди (II). Альдегиды и кетоны вступают в реакции нуклеофильного присоединения.
Строение и номенклатура карбоновых кислот
Карбоновыми кислотами называют органические вещества, содержащие в молекуле карбоксильную группу — CООН.
Общая формула карбоновых кислот R-COOH (рис. 11).
Классификация карбоновых кислот. По числу карбоксильных групп различают одноосновные (монокарбоновые), двухосновные (дикарбоновые) и т. д.
Например: CH3COOH — уксусная кислота, НООС-СООН — щавелевая кислота.

Рис. 11. Aтoмнo-орбитальная модель и распределение электронной плотности
Существуют и многоосновные карбоновые кислоты, содержащие более двух карбоксильных групп. К ним относится, например, трехосновная лимонная кислота:
В зависимости от природы углеводородного радикала карбоновые кислоты делятся на предельные, непредельные, ароматические. Общая формула ряда одноосновных насыщенных карбоновых кислот CnH2n·1COOH.
Номенклатура и изомерия. По международной номенклатуре названия кислот составляют из названий соответствующих углеводородов с прибавлением окончания -овая с добавлением слова кислота. Нумерацию углеродного скелета начинают с атома углерода карбоксильной группы.
Многие кислоты имеют и исторически сложившиеся или тривиальные, названия (табл. 3, рис. 12).
Таблица 3 Названия карбоновых кислот
| Химическая формула | Систематическое название кислоты | Тривиальное название кислоты |
| 1 | 2 | 3 |
| HCOOH | Метановая | Муравьиная |
| CH3COOH | Этановая | Уксусная |
| CH3CH3COOH | Пропановая | Пропионовая |
| CH3CH3CH3COOH | Пентановая | Валериановая |
| CH3(CH3)4COOH | Гексановая | Кахфоновая |
| CH3(CH3)6COOH | Гептановая | Энантовая |
| C16H31COOH | Гексадекановая | Пальмитиновая |
| C17H36COOH | Октадекановая | Стеариновая |

Рие. 12. Модели карбоновых кислот
а) Муравънкая кислота (метановая); в) Уксусная кислота (этановая);
в) Пропионовая кислота (пропановая)
Для карбоновых кислот возможны различные виды изомерии в зависимости от типа кислоты.
Для насыщенных одноосновных кислот характерна структурная изомерия углеродного скелета и межклассовая изомерия со сложными эфирами:
Получение. Существуют следующие способы получения карбоновых кислот.
1. Окисление первичных спиртов и альдегидов:
2. При окислении различных углеводородов также образуются карбоновые кислоты. В последнее время большое промышленное значение приобретает способ получения уксусной кислоты путем окисления бутана:
3. Гидролиз различных производных карбоновых кислот также приводит к получению кислот. Так, при гидролизе сложного эфира образуется спирт и карбоновая кислота:
В лаборатории карбоновые кислоты, как и неорганические кислоты, можно получить из их солей, действуя на них концентрированной серной кислотой при нагревании:
Карбоновыми кислотами называются производные углеводородов, содержащие в молекуле одну или несколько карбоксильных групп — COOH.
Извержение
Для эксперимента нужны: бутылка из-под газировки, противень, земля или песок, столовая ложка питьевой соды, чашка (250 мл) уксуса, красный пищевой краситель.
Поставьте бутылку на противень. Со всех сторон засыпьте бутылку землей (песком), чтобы получилась горка. Не закрывайте бутылочное отверстие и постарайтесь, чтобы земля не попала в бутылку. Насыпьте в бутылку соду. Окрасьте уксус в красный цвет и залейте его в бутылку. Наблюдайте извержение углекислого газа.
§10. СВОЙСТВА КАРБОНОВЫХ КИСЛОТ
Физические свойства. Низшие карбоновые кислоты — жидкости с характерным резким запахом, хорошо растворимые в воде. Кислоты, содержащие от 4 до 9 атомов углерода — маслянистые жидкости с неприятным запахом, содержащие более 9 атомов углерода в молекуле — твердые вещества, которые не растворяются в воде. C повышением относительной молекутлярной массы растворимость кислот в воде уменьшается, а температура кипения повышается.
Химические свойства. Для карбоновых кислот характерны те же свойства, что и для минеральных. Они взаимодействуют с металлами, стоящими в ряду активности до водорода, оксидами металлов, основаниями и солями. Во всех этих реакциях образуются соли карбоновых кислот. Соли муравьиной кислоты называются формиатами, уксусной — ацетатами, пропионовой — пропионатами. Общие свойства карбоновых кислот представлены в таблице 4.
Таблица 4 Общие свойства карбоновых кислот
Карбоновые кислоты обладают и некоторыми специфическими свойствами, обусловленными наличием в их молекулах радикалов. Так, например, уксусная кислота реагирует с хлором:
При последующем хлорировании могут быть получены и последующие хлопроизводные.
2. Муравьиная кислота по химическим свойствам несколько отличается от других своих гомологов. Из-за особенности строения молекул муравьиная кислота легко окисляется, вступая в реакцию “серебряного зеркала”:
3. При нагревании с концентрированной серной кислотой муравьиная кислота отщепляет воду и образуется монооксид углерода:
амой сильной из одноосновных карбоновых кислот является муравьиная кислота. Уксусная кислота значительно слабее. Следовательно, радикал метил CH3— (и другие радикалы) оказывает влияние на карбоксильную группу.
Как мы заметили, в радикалах карбоновых кислот атомы водорода замещаются галогенами. При этом замещение легко происходит в углеводородном звене, которое находится ближе к карбоксильной группе. Тем самым карбоксильная группа влияет на углеводородный радикал, следовательно, их влияние взаимно.
Применение. Уксусную кислоту применяют для получения пластмасс и искусственного волокна. Ацетаты различных металлов используют для окрашивания тканей. Кроме того, раствор уксусной кислоты (уксус) широко применяют в пищевой промышленности и в быту.
Муравьиная кислота обладает дезинфицирующим свойством, поэтому находит свое применение в пищевой, кожевенной и фармацевтической промышленности, в медицине. Она также используется при крашении тканей и бумаги.
Натриевые и калиевые соли высших карбоновых кислот — основные составные части мыла.
Высшие карбоновые кислоты широко используются в парфюмернокосметической промышленности, а также для получения различных моющих средств.
Одноосновные непредельные карбоновые кислоты — производные ненасыщенных углеводородов, у которых один атом водорода замещен карбоксильной группой.
Двойная связь в молекуле олеиновой кислоты расположена между атомами C9—C10:
CH3(CH3)7-CH = CH-(CH3)7COOH.
В молекуле линолевой кислоты имеются две двойные связи, и они расположены между атомами C10 и C12—C13:
CH3(CH3)3 — (CН3CH=CH)3(CH3)-COOH,
а в линолевой кислоте — между C9—C10, C12—C13 и C15—C16:
CH3(CH3CH=CH)3(CH3)7COOH.
Высшие непредельные карбоновые кислоты входят в состав растительных жиров в виде сложных эфиров глицерина.
Получение:
1. Дегидрогалогенирование галогензамещенных кислот
CH3-CH3-СНСl—СООН → CH3-CH=CH-COOH + HCl
2. Дегидратация оксикислот:
Физические свойства: Низшие непредельные кислоты — жидкости, растворимые в воде с сильным острым запахом; высшие — твердые, не растворимые в воде вещества без запаха.
при окислении образуются диоксикислоты
Для карбоновых кислот характерны те же свойства, что и для минеральных. Они взаимодействуют с металлами, стоящими в ряду активности до водорода, оксидами металлов, основаниями и солями. Во всех этих реакциях образуются соли карбоновых кислот. Самой сильной из одноосновных карбоновых кислот является муравьиная кислота. Муравьиная кислота по химическим свойствам несколько отличается от других своих гомологов. Из-за особенности строения молекул муравьиная кислота легко окисляется, вступая в реакцию “серебряного зеркала”.
Опыты с уксусной кислотой
Проделайте дома доступные опыты с уксусной кислотой, например: а) проверьте действие на мел; б) изменяет ли она окраску некоторых растительных соков.
Умей применять знания по химии.
Если потребуется отвинтить ржавую гайку, то рекомендуется вечером положить на нее тряпку, смоченную в уксусной кислоте. Утром отвинтить эту гайку будет значительно легче.
Сложные эфиры
При изучении кислот мы неоднократно встречались с их производными — сложными эфирами.
Общую формулу сложного эфира можно представить: 
Номенклатура. Названия сложных эфиров складываются от названий кислот и спиртов, остатки которых содержатся в их молекулах, например:
Изомерия сложных эфиров определяется изомерией углеводородных радикалов кислот и спиртов, составляющих сложный эфир.
Сложные эфиры изомерны предельным монокарбоновым кислотам, например:
Нахождение в природе. Сложные эфиры широко распространены в природе. Часто встречаются в растениях придавая аромат цветам, запах плодам и ягодам являются составной частью эфирных масел — апельсиновое, лавандовое, розовое и др.
Получение. Самой распространенной реакцией получения сложных эфиров является реакция этерификации, в которой взаимодействуют карбоновая кислота и спирт.
Взаимодействие карбоновых кислот со спиртами с образованием сложных эфиров называется реакцией этерификации:
Реакция этерификации обратима. В реакции обратной этерификации, которая называется гидролизом сложного эфира, образуются кислота и спирт:
Реакция проводится в присутствии концентрированной серной кислоты:
Сложные эфиры образуются также при взаимодействии минеральных кислот со спиртами, например при нитровании глицерина.
Физические свойства. Сложные эфиры одноосновных карбоновых кислот — жидкости с приятным запахом, легче воды, летучие. Например, бутиловый эфир масляной кислоты имеет запах ананаса, метиловый эфир масляной кислоты — запах яблок, изобутиловый эфир уксусной кислоты — запах бананов. Температуры кипения и плавления сложных эфиров ниже, чем соответствующих органических кислот.
Химические свойства. Важнейшим химическим свойством сложных эфиров является взаимодействие их с водой (гидролиз).
Гидролиз является реакцией обратной реакции этерификации, протекает в кислой или щелочной среде:
Реакцию гидролиза сложного эфира называют омылением.
Применение. Сложные эфиры очень широко применяют в качестве органических растворителей. Эфиры также применяют в качестве добавок при производстве освежающих напитков, конфет и других пищевых продуктов, а также в парфюмерии (рис. 13).
Сложные эфиры — функциональные производные y карбоновых кислот.
Общую формулу сложного эфира можно представить: 
Самой распространенной реакцией получения сложных эфиров является реакция этерификации, в которой взаимодействуют карбоновая кислота и спирт.
Жиры
Жиры — природные соединения, которые представляют собой сложные эфиры глицерина и высших карбоновых кислот.
Строение жиров. Строение жиров было установлено благодаря трудам французских химиков Шеврёля и Бертло. При нагревании жиров с водой (в щелочной среде) в начале XIX в. Э. Шеврёль установил, что жиры расщепляются и образуются глицерин и различные карбоновые кислоты (стеариновая, олеиновая и др.). М. Бертло осуществил обратную реакцию: при нагревании глицерина с высшими карбоновыми кислотами он получил жиры и воду.
Мишель Эжен Шеврёль
Впервые химический состав жиров определил в начале прошлого века французский химик Мишель Эжен Шеврёль.
На основании этих экспериментов сделали вывод: жиры — это сложные эфиры глицерина и карбоновых кислот (триглицериды).
Общую формулу жира можно представить в виде:
Большинство жиров образовано тремя карбоновыми кислотами: олеиновой C17H33COOH, пальмитиновой C15H31COOH и стеариновой C17H35COOH.
В обычных условиях жиры, содержащие в своем составе остатки непредельных кислот, чаще всего бывают жидкими. Их называют маслами. В основном это жиры растительного происхождения — льняное, подсолнечное и др. Реже встречаются жидкие жиры животного происхождения, например, рыбий жир. Большинство природных жиров животного происхождения при обычных условиях твердые вещества и содержат в основном остатки предельных карбоновых кислот, например, бараний жир. Однако, пальмовое масло твердое в обычных условиях — жир (рис. 14).
Общее название жиров триглицериды.

М. Бертле (1857-1907)
В 1854 г. французский химик Марселен Бертло провел реакцию этерификации между глицерином и жирными кислотами и таким образом впервые синтезировал жир.
Физические свойства. Природные жиры не имеют конкретной температуры плавления (“точки плавления”), они предварительно размягчаются и плавятся в определенном интервале температуры. Температура затвердевания жира тем выше, чем больше в нем содержание остатков предельных кислот. Жиры легко растворяются в органических растворителях и практически не растворяются в воде.
Химические свойства. Химические свойства жиров определяются принадлежностью их к классу сложных эфиров, поэтому для них характерна реакция — гидролиз. Гидролиз жиров происходит в кислой или щелочной среде при повышенной температуре.
Кислотный гидролиз приводит к образованию карбоновых кислот и глицерина: 
Рис. 14. Твердые и жидкие жиры
Щелочной гидролиз (омыление жиров) приводит к образованию солей жирных кислот (мыла) и глицерина:
Триглицериды, содержащие остатки непредельных кислот, подвергаются гидрированию. В промышленности гидрирование жидких жиров используется для превышения их в более ценные твердые жиры (саломас).
Таким образом, из растительного масла в промышленности получают маргарин.
Применение. Жиры — важнейшая часть пищи человека. В организме человека он подвергается гидролизу, а продукты гидролиза используются для синтеза жиров, свойственных данному организму. Питательная ценность жиров выше, чем углеводов и белков. При окислении 1 г жира выделяется примерно 39 кДж энергии. Жиры в организме служат резервным питательным веществом, а также выполняют защитную и теплоизоляционную функции.
Кроме того, жиры применяются для получения глицерина, высших карбоновых кислот, мыла.
Жиры — природные соединения, которые представляют собой сложные эфиры, глицерина и высших карбоновых кислот. Жиры бывают твердые и жидкие (масло), животного и растительного происхождения. Твердые жиры образованы преимущественно высшими предельными карбоновыми кислотами, а жидкие жиры образованы высшими непредельными карбоновыми кислотами. В промышленности гидрирование жидких жиров используется для превращения их в более ценные твердые жиры. Жиры — важнейшая часть пищи человека.
Изготовим духи.
Для создания ведущего запаха понадобится прежде всего цитрусовое масло, которое мы получим из кожуры лимонов или апельсинов. Натрем кожуру этих фруктов на терке, в протертом виде завернем в кусочек прочной материи и тщательно выдавим. Через ткань пройдет мутная жидкость, состоящая из эфира и воды. Смешаем приблизительно 2 мл этой жидкости с каплями ландышевого масла, ванильного сахара, масла еловых веток. Затем растворим полученную смесь в 20 мл спирта. Духи готовы!
Проделайте дома следующие опыты: а) выведите при помощи бензина жирные пятна с одежды; б) сравните ценообразование обычного мыла и синтетического моющего порошка в жесткой воде; в) произведите смягчение воды добавкой соды и кипячением и проверьте результаты.
Мыла и синтетические моющие средства
Мыла — это соли высших карбоновых кислот. Обычные мыта состоят главным образом из смеси пальмитиновой, стеариновой и олеиновой кислот. Натриевые соли образуют твердые мыла, калиевые соли — жидкие мыла.
Мыла получаются при гидролизе жиров в присутствии щелочей.
Жир + щелочь = соли жирных кислот и глицерин.
Например:
Отсюда реакция, обратная этерификации получила названия реакции омыления. Омыление — это гидролиз сложных эфиров под действием щёлочи. Омыление жиров может протекать и в присутствии серной кислоты (кислотное омыление). При этом получаются глицерин и высшие карбоновые кислоты. Последние действием щелочи или соды переводят в мыла.
Исходным сырьем для получения мыла служат растительные масла (подсолнечное, хлопковое и др.), животные жиры, а также гидроксид натрия или кальцинированная сода. Растительные масла предварительно подвергаются гидрогенизации, т.е. их превращают в твердые жиры. Применяются также заменители жиров — синтетические карбоновые жирные кислоты с большой молекулярной массой.
Производство мыла требует больших количеств сырья, поэтому поставлена задача получения мыла из непищевых продуктов. Необходимые для производства мыла карбоновые кислоты получают окислением парафина. Нейтрализацией кислот, содержащих от 10 до 16 углеродных атомов в молекуле, получают туалетное мыло, а из кислот, содержащих от 17 до 21 атома углерода, — хозяйственное мыло и мыло для технических целей. Мыло, получаемое из жиров, плохо моет в жесткой воде. Поэтому наряду с мылом из синтетических кислот производят синтетические моющие средства (CMC) из других видов сырья, например из алкилсульфатов — солей сложных эфиров высших спиртов и серной кислоты.
В общем виде образование таких солей можно изобразить уравнениями:
Эти соли содержат в молекуле от 12 до 14 углеродных атомов и обладают очень хорошими моющими свойствами. Кальциевые и магниевые соли растворимы в воде, а потому такие мыла моют и в жесткой воде. Алкилсульфаты содержатся во многих стиральных порошках.
Синтетические моющие средства высвобождают сотни тысяч тонн пищевого сырья — растительных масел и жиров.
Свойства мыла. Поверхностный слой дистиллированной воды находится в натянутом состоянии подобно упругой пленке. При добавлении мыла и некоторых других растворимых в воде веществ поверхностное натяжение воды уменьшается. Мыло и другие моющие вещества относят к поверхностно-активным веществам (ПАВ). Они уменьшают поверхностное натяжение воды, усиливая тем самым моющие свойства воды (рис. 15).

Рис 15
Молекулы ПАВ на пограничной поверхности располагаются так, что гидрофильные группы карбоксильных анионов направлены в воду, а углеводородные гидрофобные выталкиваются из нее (рис. 16). Такая водная поверхность имеет меньшее поверхностное натяжение, что способствует быстрому и полному смачиванию загрязненных поверхностей.

Рис 16
Использование чрезмерного количества этих средств приводит к загрязнению окружающей среды. Многие ПАВ трудно поддаются биологическому разложению. Поступая со сточными водами в реки и озера, они загрязняют окружающую среду. В результате образуются целые горы пены в канализационных трубах, реках, озерах, куда попадают промышленные и бытовые стоки. Использование некоторых ПАВ приводит к гибели всех живых обитателей в воде.
В состав мыла входят соли пальмитиновой, стеариновой кислот. Растворимость мыла в воде связана с наличием в его составе катиона металла.
CMC (синтетические моющие средства) — натриевые соли синтетических кислот. CMC в основном состоят из алкилсульфатных солей натрия RO—SO2—ONa. R — углеводородный радикал, имеющий в составе от 8 до 18 атомов углерода.
III глава Самое важное
• Алвдегидьг и кетоны содержат функциональную группу — карбонил C=O. Альдегиды имеют рядом с такой группой еще один другой атом углерода, а в кетонах данная группа соединена с другими двумя атомами углерода.
• Альдегиды и кетоны вступают в реакцию гидрирования образуя при этом: Альдегиды — первичные спирты;
Кетоны — вторичные спирты.
• Альдегиды окисляются до карбоновых кислот, а кетоны окисляются только сильными окислителями до нескольких кислот.
• Альдегиды и кетоны вступают в реакции нуклеофильного присоединения с синильной кислотой и гидросульфитом натрия.
• Альдегидам характерна качественная реакция “серебряного зеркала” с реактивом Толленса, в которой образуется серебро, а также с реактивом Фелинга, в которой образуется красный осадок оксида меди (+1). Кетоны в данные реакции не вступают.
• Все карбоновые кислоты являются слабыми кислотами и электролитами. Они проявляют общие свойства кислот (реагируют с металлами, их оксидами и гидроксидами, солями), а также проявляют свойства органических веществ (например, этерификацию, замещение с галогенами, разложение и окисление).
• Важнейшими представителями сложных эфиров являются жиры. Жиры образованные непредельными кислотами (растительные масла), и предельными кислотами (животные жиры). Наиболее важными свойствами жиров являются реакции гидролиза и гидрирования (образование маргарина).
Муравьиная кислота по строению и свойствам отличается от остальных карбоновых кислот.
1) В молекуле муравьиной кислоты вместо углеводородного радикала присутствует атом водорода. По этой причине эта кислота является более сильной.
2) В молекуле муравьиной кислоты наряду с карбоксильной группой можно выделить также альдегидную группу. 
Поэтому вступает с реакции, характерные как для кислот, так и для альдегидов.
Услуги по химии:
Лекции по химии:
Лекции по неорганической химии:
Лекции по органической химии:
Присылайте задания в любое время дня и ночи в ➔ 
Официальный сайт Брильёновой Натальи Валерьевны преподавателя кафедры информатики и электроники Екатеринбургского государственного института.
Все авторские права на размещённые материалы сохранены за правообладателями этих материалов. Любое коммерческое и/или иное использование кроме предварительного ознакомления материалов сайта natalibrilenova.ru запрещено. Публикация и распространение размещённых материалов не преследует за собой коммерческой и/или любой другой выгоды.