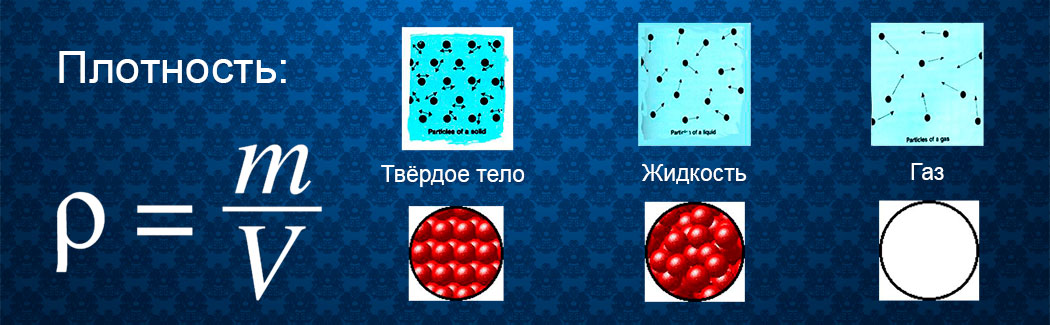
Как перевести плотность в проценты
Что делать с этими процентами? Или как перевести % в граммы и наоборот — число в проценты!
Как перевести проценты в граммы и наоборот
Чувствую, назрела острая необходимость осветить эту животрепещущую и важную тему для всех, кто занимается изготовлением мыла с нуля и домашней косметикой (а также печёт хлеб и занимается прочей деятельностью, связанной с рецептурой 🙂
Уже несколько раз я сталкивалась с недоуменным вопросом своих читателей:
или наоборот:
Конечно же, нет ничего проще! Вы удивитесь, насколько легко и быстро научиться переводить проценты в граммы, а числа переводить в проценты!
Шаг 1. Сначала разберёмся с маслами.
У нас по рецепту 80% оливкового масла и 20% бабассу баттер.
Процент означает сотую долю числа, это значит, что если мы видим обозначение 80%, это равно 0.8 в десятичной дроби.
Т.е. 80 разделить на 100 = 0.8
Соответственно, 20%=20/100=0.2
А 100%=100%/100 = 1.0
Сумма масел в рецепте должна составлять 100%, что мы и видим тут: 80%+20%=100%
Если у вас просто рецепт в процентах и нигде не указано, что дополнительно нужно добавить какие-то ингридиенты, то сумма всего рецепта должна составлять 100%!
В случае с мылом мы всегда указываем в % вес масел (?масел=100%). И дополнительно к нему считаем щёлочь и другие добавки).
Шаг 2. Вернёмся к рецепту. Допустим, вы решили сварить мыло на 500 грамм масел.
Тогда, чтобы составить рецепт, вам необходимо умножить 80% (0.8) оливкового масла на общий вес масел и 20% (0.2) бабассу баттер на общий вес масел:
оливковое масло: 0.8*500 = 400 грамм
бабассу баттер : 0.2*500 = 100 грамм
итого: 500 грамм
Теперь вы знаете, сколько вам нужно масел, и хватит ли вам их, если вы хотите воспользоваться данным рецептом!
Шаг 3. Далее считаем воду и щёлочь по калькулятору щёлочи, как это сделать, подробно написано тут: http://magicsoap.ru/calculator/
Шаг 4. Если в рецепте мыла написаны ещё какие-то ингридиенты в %, то это означает, что их мы должны добавить дополнительно к весу масел. Как это рассчитать? Легко!
Вес масел, как мы помним, 500 г, дополнительно мы должны добавить 0,5% шелковых нитей и 3% лимонной кислоты:
1) переводим проценты в число:
0.5%= 0.5/100=0.005
3%=3/100=0.03
2) умножаем вес масел (от которых мы высчитываем массу добавок) на получившееся от процентов число:
0.005*500 = 2.5 грамма шелковых ниток
0.03*500 = 15 грамм лимонной кислоты
Вот и всё! Ваш рецепт мыла в граммах будет выглядеть так:
А теперь — обратный вариант!
Шаг 1. Считаем общую массу ингридиентов и принимаем её за 100%
8+7+9+160+16 = 200 грамм это 100%
Шаг 2. Вычисляем долю каждого ингридиента в общей массе
Для это нужно разделить вес каждого ингридиента на общую массу рецепта. Так мы вычислим долю каждого ингридиента в рецепте.
8 разделить на 200 = 0,04
7 разделить на 200 =0,035
9 разделить на 200 = 0,045
160 разделить на 200 = 0,8
16 разделить на 200 = 0,08
Общая сумма должна быть равна 1!
Шаг 3. Переводим десятичную дробь (долю) — в проценты!
Для этого получившееся выше число нужно умножить на 100 и приписать значок %
0,04*100%=4%
0,035*100%=3,5%
0,045*100%=4,5%
0,8*100%=80%
0,08*100%=8%
Вот и всё, ваш рецепт в % будет выглядеть так:
Теперь вы знаете всё: как перевести число в проценты, как перевести цифры в проценты, как перевести проценты в доли и т.д.!
Пересчитываем концентрации растворов из одних единиц в другие
При пересчете процентной концентрации в молярную и наоборот, необходимо помнить, что процентная концентрация рассчитывается на определенную массу раствора, а молярная и нормальная – на объем, поэтому для пересчета необходимо знать плотность раствора. Если мы обозначим: с – процентная концентрация; M – молярная концентрация; N – нормальная концентрация; э – эквивалентная масса, ρ – плотность раствора; m – мольная масса, то формулы для пересчета из процентной концентрации будут следующими:
Этими же формулами можно воспользоваться, если нужно пересчитать нормальную или молярную концентрацию на процентную концентрацию.
Мольная масса серной кислоты равна 98. Следовательно,
Подставляя необходимые значения в формулы, получим:
а) Молярная концентрация 12% раствора серной кислоты равна
M = (12 × 1,08 × 10) / 98 = 1,32 M
б) Нормальная концентрация 12% раствора серной кислоты равна
N = (12 × 1,08 × 10) / 49 = 2,64 H.
Иногда в лабораторной практике приходится пересчитывать молярную концентрацию в нормальную, и наоборот. Если эквивалентная масса вещества равна мольной массе (например, для HCl, KCl, KOH), то нормальная концентрация равна молярной концентрации. Так, 1 Н раствор соляной кислоты будет одновременно 1 M раствором. Однако, для большинства соединений эквивалентная масса не равна мольной и, следовательно, нормальная концентрация растворов этих веществ не равна молярной концентрации.
Для пересчета из одной концентрации в другую можно использовать формулы:
Вычислить нормальную концентрацию 1 М раствора серной кислоты.
Вычислить молярную концентрацию 0,5 н Na2CO3
M = (0,5 × 53) / 106 = 0,25 M
Ссылка на источник
01.09.2021 11:09:35 | Автор статьи: Усачёва Вера
Концентрация растворов. Способы выражения концентрации растворов.
Концентрация раствора может выражаться как в безразмерных единицах (долях, процентах), так и в размерных величинах (массовых долях, молярности, титрах, мольных долях).
Способы выражения концентрации растворов.
1. Массовая доля (или процентная концентрация вещества) – это отношение массы растворенного вещества m к общей массе раствора. Для бинарного раствора, состоящего из растворённого вещества и растворителя:

ω – массовая доля растворенного вещества;
mв-ва – масса растворённого вещества;
Массовую долю выражают в долях от единицы или в процентах.
2. Молярная концентрация или молярность – это количество молей растворённого вещества в одном литре раствора V:

C – молярная концентрация растворённого вещества, моль/л (возможно также обозначение М, например, 0,2 М HCl);
n – количество растворенного вещества, моль;
V – объём раствора, л.
Раствор называют молярным или одномолярным, если в 1 литре раствора растворено 1 моль вещества, децимолярным – растворено 0,1 моля вещества, сантимолярным – растворено 0,01 моля вещества, миллимолярным – растворено 0,001 моля вещества.
3. Моляльная концентрация (моляльность) раствора С(x) показывает количество молей n растворенного вещества в 1 кг растворителя m:

С (x) – моляльность, моль/кг;
n – количество растворенного вещества, моль;
4. Титр – содержание вещества в граммах в 1 мл раствора:

T – титр растворённого вещества, г/мл;
mв-ва – масса растворенного вещества, г;
5. Мольная доля растворённого вещества – безразмерная величина, равная отношению количества растворенного вещества n к общему количеству веществ в растворе:

N – мольная доля растворённого вещества;
n – количество растворённого вещества, моль;
nр-ля – количество вещества растворителя, моль.
Сумма мольных долей должна равняться 1:
Иногда при решении задач необходимо переходить от одних единиц выражения к другим:
М(Х) – молярная масса растворенного вещества;
ρ= m/(1000V) – плотность раствора. 6. Нормальная концентрация растворов (нормальность или молярная концентрация эквивалента) – число грамм-эквивалентов данного вещества в одном литре раствора.
Грамм-эквивалент вещества – количество граммов вещества, численно равное его эквиваленту.
Эквивалент – это условная единица, равноценная одному иону водорода в кислотоно-основных реакциях или одному электрону в окислительно – восстановительных реакциях.
Для записи концентрации таких растворов используют сокращения н или N. Например, раствор, содержащий 0,1 моль-экв/л, называют децинормальным и записывают как 0,1 н.

СН – нормальная концентрация, моль-экв/л;
z – число эквивалентности;
Коэффициент растворимости – отношение массы вещества, образующего насыщенный раствор при конкретной температуре, к массе растворителя:
Формулы для пересчета концентраций растворов
В приводимой ниже таблице приняты следующие обозначения:
М — мольная масса растворенного вещества, г/моль; Э — эквивалентная масса растворенного вещества, г/моль; р — плотность раствора, г/мл.
* Дли жидкостей может применяться величина Pv, % (об.) —число миллилитров растворенной жидкости в 100 мл раствора.
РАСЧЕТНЫЕ ФОРМУЛЫ, ИСПОЛЬЗУЕМЫЕ ДЛЯ ПРИГОТОВЛЕНИЯ РАСТВОРОВ
Для приготовления определенного количества раствора какого-либо вещества заданной концентрации исходят из следующих данных: а) из количества чистого вещества и растворителя; б) из количества раствора данного вещества с более высокой концентрацией, чем заданная, и количества чистого растворителя или в) из количества двух растворов того же вещества, один из которых имеет концентрацию больше нужной, а другой — меньше.
Растворение вещества в воде
Пусть требуется приготовить А граммов раствора концентрации P [в % (масс.) ]. Тогда:
(I) 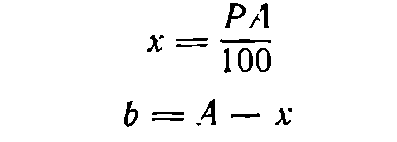
(2)
где х— необходимая масса растворяемого вещества, г; b—необходимая масса воды, г.
Если нужно приготовить определенный объем V раствора (в мл) концентрации Р, находят по таблицам плотность р (в г/см3) раствора данного вещества требуемой концентрации. Поскольку А = Vp, формула (1) будет иметь вид:
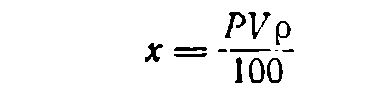
(3)
В тех случаях, когда растворяемое вещество представляет собой кристаллогидрат, т. е. содержит кристаллизационную воду, для расчета необходимого его количества используют формулу:
(4) 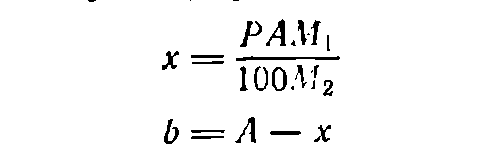
(5)
где х— необходимая масса кристаллогидрата, г; M1—мольная масса кристаллогидрата; М2—моль-мая масса вещества без кристаллизационной воды; b — необходимая масса воды, г.
Если нужно приготовить раствор объемом V (в мл) заданной нормальности N, вычисляют значение эквивалентной массы Э растворяемого вещества, после чего находят необходимую его навеску (в г) по формуле:
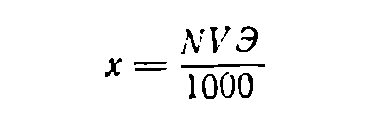
(6)
При приготовлении раствора заданной молярной концентрации применяют аналогичную формулу:
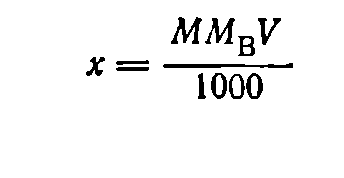
(7)
где М — молярная концентрация раствора; Мв — мольная масса растворяемого вещества; V — заданный объем раствора, мл.
Разбавление раствора водой
Пусть требуется приготовить раствор концентрации Р2 из имеющегося раствора с более высокой концентрацией Р1. Обозначим массу раствора до разбавления А1, а массу раствора после разбавления— А2. Тогда массу воды b (в г), необходимую для разбавления, находят по формуле (8) или (9) в зависимости от того, задано ли значение А\ или А2.
(9) 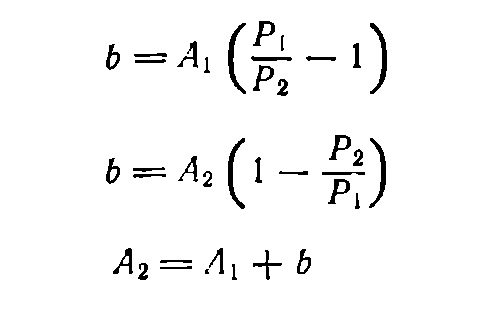
(10)
В тех случаях, когда известна не масса, а объем раствора, необходимо по таблицам найти плотности растворов данного вещества исходной и конечной концентраций — p1 и р2 соответственно. Тогда, если нужно приготовить раствор объемом V2 (в мл) концентрации Р2 [в % (масс.)], а концентрация исходного раствора равна P1 [(в % (масс.)], то объем исходного раствора вычисляется по формуле:
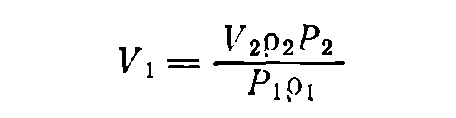
(11)
Смешивание двух растворов различной концентрации
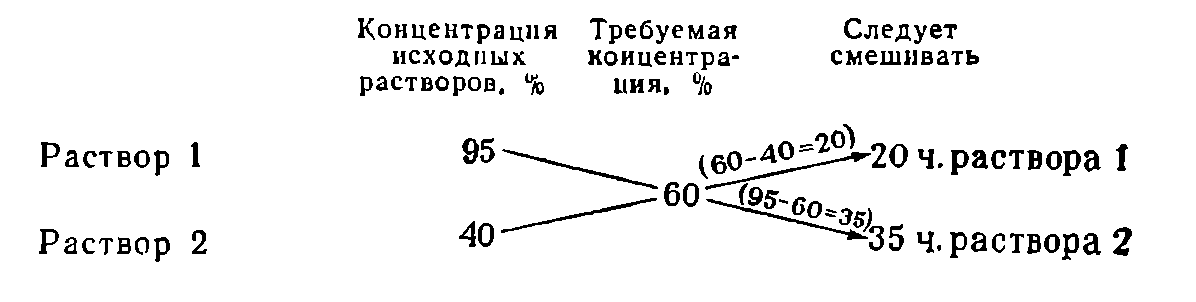
Пусть требуется приготовить раствор заданной концентрации из двух растворов того же вещества, один из которых имеет концентрацию больше нужной, а другой — меньше. Чтобы определить, в каких пропорциях следует смешивать растворы, пользуются «правилом креста», которое наглядно показано на следующем примере:
Смешиваемые растворы можно измерять в объемных или массовых частях в зависимости от того, в объемных или массовых процентах выражают концентрацию растворов.
«Правило креста» можно применять и в случаях разбавления раствора чистым растворителем. При этом концентрацию вещества в чистом растворителе считают равной нулю:
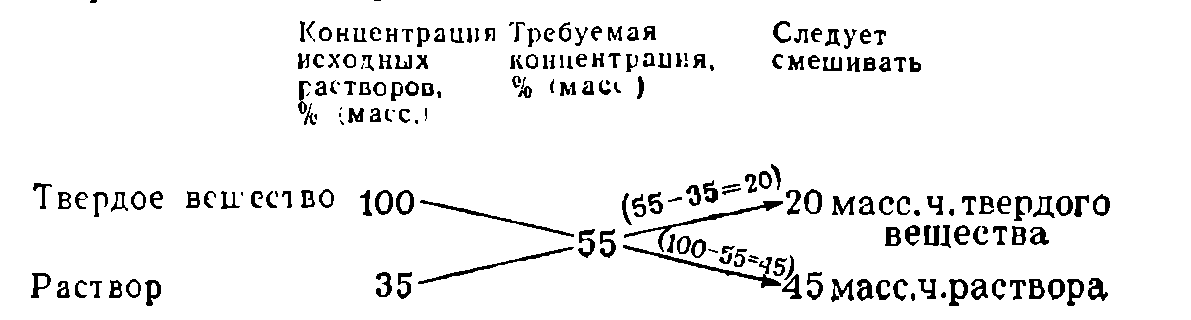
Для получения более концентрированного раствора растворением в нем дополнительного количества компонента твердое вещество условно считают раствором с концентрацией 100%:
Онлайн конвертер плотности, формулы расчета и единицы измерения
Любое тело состоит из определенного количества молекул, где каждая имеет свою массу. Таким образом, масса тела — это сумма масс молекул из которых оно состоит. Независимо от того, где находится это тело, в нем всегда одинаковое количество молекул и его масса не меняется. В разных веществах и материалах концентрация молекул сильно отличается. Их масса в единице объема — это плотность. Стандартно она измеряется в кг / м 3. Если необходимо перевести в другие величины, то проще всего использовать конвертер плотности.
Что такое плотность и как ее рассчитать
Плотность вещества — это его масса в единице объема. Плотность — уникальное физическое свойство, которое стало основой для великого открытия Архимеда — его знаменитого закона: на тело, погруженное в жидкость действует выталкивающая сила, которая равна массе вытесненной жидкости.
Здесь плотность играет решающую роль — чем она больше, тем больше тело будет погружаться. Плотность и твердость — разные понятия. Хороший пример этому вода и лед. У воды плотность больше чем у льда, поэтому он всплывает на ее поверхность, а не тонет.
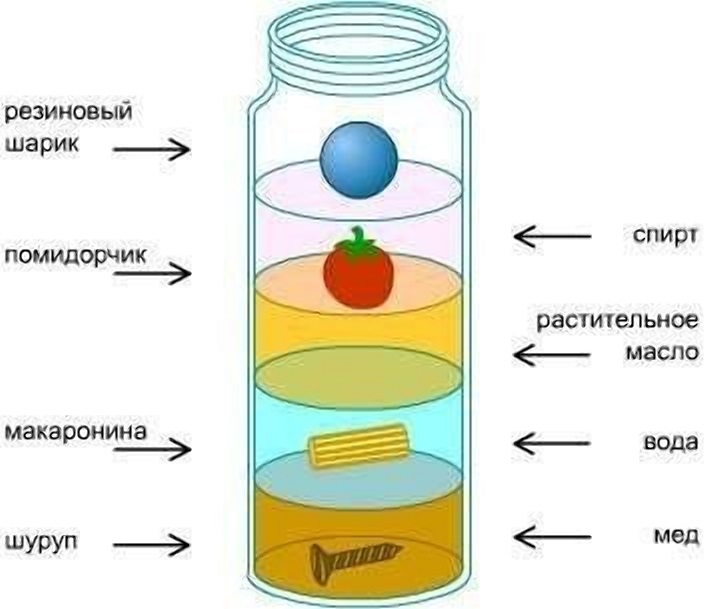
Наглядный пример этому — простой эксперимент «Башня плотности». Он доступен для проведения в домашних условиях.
Плотность обозначают символом ρ, в химии можно встретить ее обозначение буквой d латинского алфавита.
Для ее расчета используют следующую формулу: ρ = m/V, где:
ρ = плотность тела, m = его масса, V = объем.
Единицы измерения плотности
Официальной единицей измерения плотности в системе СИ является кг/м³. Поскольку это довольно большой объем, то для удобства чаще всего используют
Плотность воды составляет примерно 1 грамм / кубический сантиметр. Она принимается за стандартное значение для расчетов.
Другие единицы измерения плотности
В качестве других единиц измерения плотности, также используются метрические тонны и литры, хотя они не включены в Международную систему СИ. Другие единицы включают:
Чтобы сделать быстрый и точный перевод из одних величин в другие вы можете использовать наш конвертер плотности.
Применение понятия плотности
В нашей реальной жизни знания о плотности материалов находят широкое практическое применение. Например, при сооружении трубопроводов, в судостроении, при расчете и распределении веса в самолете и др.
Напомним: в физике плотность определяет массу вещества в единице объема, поэтому она связана с его «весом», а не с его текучестью (вязкостью).
Примеры плотности разных веществ
Вода имеет плотность 1000 кг / м³ (т.е. 1 г / см³). Это не совпадение. Исторически сложилось так, что один литр воды, при четырех градусах Цельсия при нормальном давлении, считался эталоном 1 кг массы.
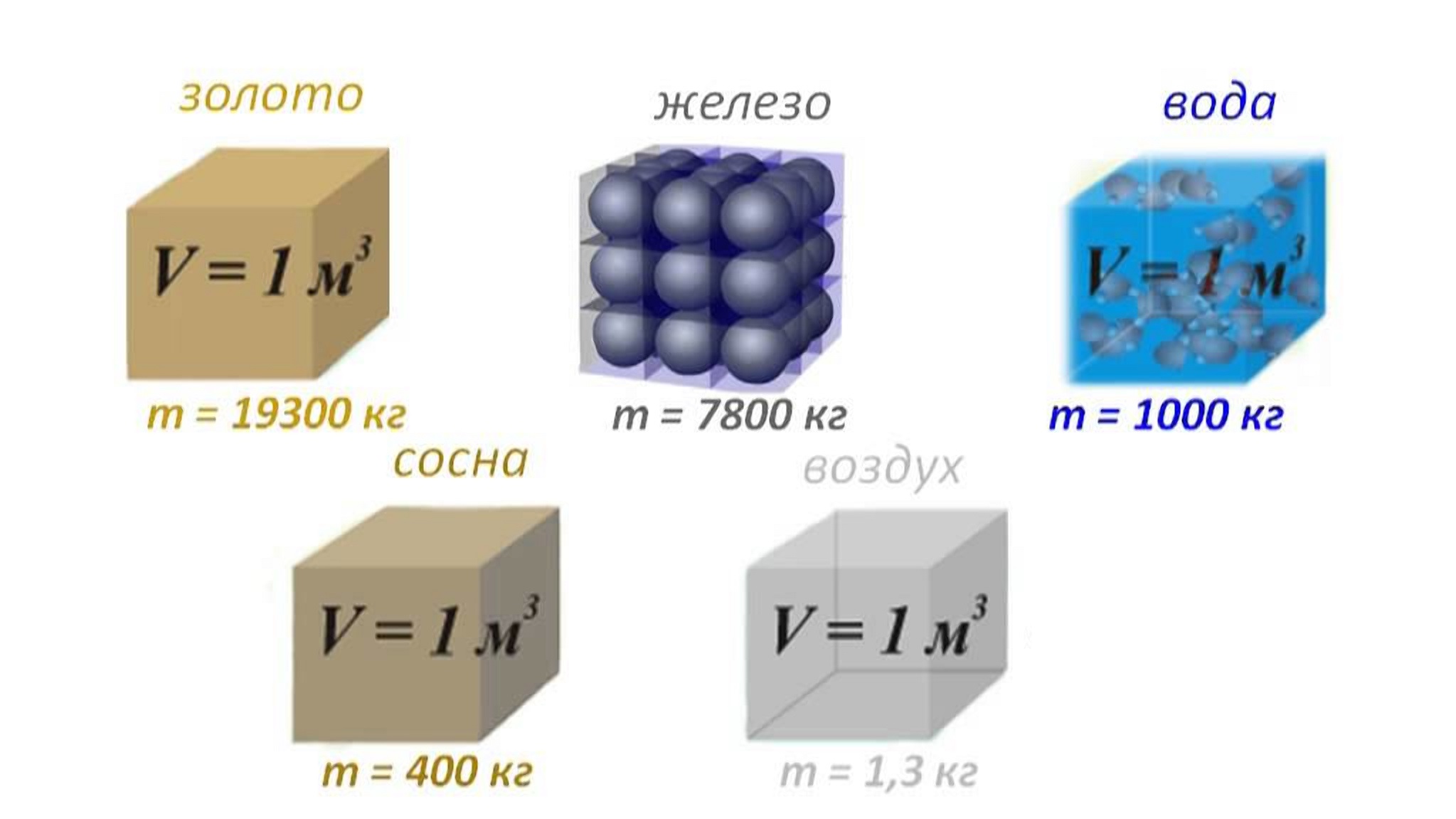
Железо, платина, золото и свинец — материалы с высокой плотностью. Многие виды горных пород и минералов также являются очень плотными. Чаще всего они отличаются большим весом и твердостью. Противоположность им — это разреженный материал, например, бамбук, алюминий или пенополистирол.
Как правило, жидкости менее плотны, чем твердые тела, а газы — чем жидкости. Это связано с тем, что твердые тела имеют плотно прилегающие частицы, в жидкостях частицы могут скользить друг вокруг друга, а в газах они свободно перемещаются.
Какая плотность у различных твердых материалах, жидкостях и газах, вы узнаете из наших таблиц.
Таблица1. Плотность твердых веществ при стандартной температуре 20 ° C
| кг/м³ | |
| графит | 2300–2720 |
| гипс | 2320 |
| кремний | 2330 |
| бериллий | 2700 |
| алюминий | 2720 |
| кварц | 2300–2700 |
| цинк | 7131 |
| медь | 8960 |
| латунь | 8200–8950 |
| платина | 21 410 |
| нержавеющая сталь | 8100 |
| золото | 19 320 |
| тополь | 350–400 |
| липа | 320–590 |
| сосна | 370–600 |
| дубовая древесина | 600–900 |
| кованое железо | 7800–7900 |
| лед (0 ° C) | 920 |
| каменная соль | 2160 |
Таблица 2. Плотность жидкостей
| кг/м³ | |
| этанол | 791 |
| жидкий азот (–196 ° C) | 808 |
| бензин | 700 |
| эфир | 720 |
| глицерин | 1260 |
| масло | 800 |
| ртуть | 13 550 |
| дистиллированная вода (4 ° C) | 1000 |
| жидкий водород (–253 ° C) | 71 |
Таблица 3. Плотность газов при стандартном атмосферном давлении 101325 Па
| Газы | кг/м³ |
| аргон | 1,784 |
| азот | 1,250 |
| хлор | 3,22 |
| углекислый газ | 1,98 |
| этан | 1,36 |
| гелий | 0,178 |
| метан | 0,717 |
| воздух | 1,293 |
| кислород | 1,429 |
| водород | 0,09 |
Простое объяснение физического понятия о плотности веществ вы найдете в нашем видео.
Онлайн конвертер объема, единицы и системы измерения, конвертация величин объема
Онлайн конвертер площади, единицы измерения площади в разных системах, их быстрый перевод
Онлайн конвертер длины, перевод всех систем измерения, метрическая, британо-американская, старорусская, морская, астрономическая, типографская
Онлайн конвертер долей, перевод дюжин, процентов, промилле и других единиц
Конвертер температур, перевод градусов Цельсия, Фаренгейта, Кельвина, Реомюра
Расход затирки для плитки на 1 м 2 — калькулятор, формула расчета